ХГЧ и его роль в диагностике онкологических заболеваний – расшифровка анализов на Онкофоруме

Это соединение защищает эмбрион от враждебной реакции иммунной системы матери и способствует выработке гормонов, необходимых для поддержания беременности. После 8-10 недели, когда сформируется плацента, ХГЧ постепенно снижается и после 20 недели остается на одном уровне до самых родов.
Для наблюдения за уровнем ХГЧ существуют специальные таблицы, где показано его количество в зависимости от срока беременности. И при каком-либо отклонении от этих данных стоит провести более подробное обследование, чтобы не пропустить возможных осложнений или новообразований.
У небеременных женщин и мужчин ХГЧ вырабатывается в небольшом количестве в гипофизе (часть мозга, участвующая в гормональной регуляции организма) и в незрелых клетках эпителия.Нормальное содержание ХГЧ в сыворотки человека до 5 МЕ/мл и до 10 МЕ/мл у женщин в постменопаузе, однако, при некоторых заболеваниях (и онкологических в частности) уровень гонадотропина может изменяться в ту или иную сторону.
О чем может говорить низкий уровень ХГЧ
Низкий уровень ХГЧ будет тревожным признаком только у беременных женщин. В случае, когда уровень гонадотропина у беременных ниже положенного при соответствующем сроке, это может стать поводом для тщательного обследования, так как такое снижение ХГЧ бывает при некоторых патологиях беременности и плода. У небеременных женщин и мужчин отрицательный результат теста на ХГЧ является вариантом нормы.
Причины повышения уровня ХГЧ
Также увеличение уровня ХГЧ наблюдается при хорионкарциноме. Данная патология очень часто возникает после пузырного заноса или медицинского аборта. Клетки хорионэпителиомы также могут продуцировать ХГЧ, что и будет являться одним из критериев для диагностики заболевания.
У мужчин при раке яичек тоже определяется ХГЧ. Это связанно с тем, что новообразование содержит эмбриональные ткани, которые и продуцируют этот онкомаркер.
При раке яичников и раке матки возможно наличие клеток, вырабатывающих ХГЧ. В частности, это будет встречаться при герминогенных опухолях.
Однако ХГЧ будет специфичным онкомаркером не только для новообразований половой системы. Его уровень будет расти при некоторых видах рака печени, почек, желудка, поджелудочной железы, толстого и тонкого кишечника, легкого, что будет связано с продуцированием ХГЧ зародышевыми клетками, из которых состоят эти виды онкологических образований. Кроме того, гонадотропин будет увеличен при сахарном диабете беременных.
Подготовка к анализу и способ определения ХГЧ
Уровень ХГЧ определяют в сыворотке крови и в моче. Для исследования ХГЧ в сыворотке необходимо взять на анализ венозную кровь. Существуют некоторые правила для правильной сдачи этого анализа.
Во-первых, кровь на ХГЧ нужно сдавать строго натощак, желательно после восьмичасового голодания, в утренние часы.
Во-вторых, стоит прекратить прием каких-либо лекарственных средств за одну-две недели до сдачи анализа, так как некоторые препараты могут повлиять на уровень ХГЧ в крови.
В-третьих, не рекомендуется за день перед анализом заниматься физической нагрузкой и иметь половой контакт.
И, в-четвертых, за сутки до взятия крови необходимо отказаться от жирной и жареной пищи.
Для определения ХГЧ в сыворотке крови и моче применяется иммуннохимический метод, который заключается в том, что к сыворотке или моче, содержащей онкомаркер, добавляется вещество с антителами к ХГЧ. Эти антитела образуют химические соединения с антигенами (ХГЧ), впоследствии выявляемые в лабораторных условиях. Стоит заметить, что в сыворотке крови присутствуют соединения, приводящие к возможным ложноположительным и ложноотрицательным результатам анализа. Эти соединения могут реагировать с антителами вместо ХГЧ, что будет приводить к ошибкам обследования. Поэтому в сомнительных случаях для диагностики и мониторинга (наблюдения) пациентов с новообразованиями определяют уровень гонадотропина в моче.
Роль ХГЧ в диагностике онкологических заболеваний
ХГЧ обладает 100% чувствительностью в диагностике герминогенных опухолей, хорионкарцином и различных видов новообразований мочеполовой системы, желудочно-кишечного тракта, возникающих из зародышевых клеток.
Уровень гонадотропина при пузырном заносе увеличен в 3-5 раз, причем он не будет снижаться после 10 недели беременности, оставаясь на высоком уровне. После удаления пузырного заноса ХГЧ постепенно снизится, однако за его уровнем необходимо будет следить некоторое время, чтобы исключить развитие хорионкарциномы. Также для исключения появления злокачественных процессов ХГЧ определяют через 40 дней после аборта.
Онкомаркер подходит также для того, чтобы диагностировать рак яичек и отличить его от доброкачественного заболевания – эпидидимита.
Анализ на ХГЧ применяют в комплексе с другими методами диагностики и другими онкомаркерами (ультразвуковое исследование, МРТ, СКТ, рентгенологическое исследование и другие). Анализ на хорионический гонадотропин используется для наблюдения за теми пациентами, которые уже получают лечение или получали его в прошлом. Таким образом проводится мониторинг их состояния и прогнозируется дальнейшее течение заболевания. В этом случае, чем выше уровень онокмаркера, тем хуже прогноз. Отрицательный ХГЧ будет означать успешное излечение заболевания. После лечения ХГЧ может увеличиваться при рецидиве заболевания, метастазировании. Однако повышение гонадотропина также может свидетельствовать и о распаде опухоли.
Для лучшего наблюдения за пациентами анализ на ХГЧ необходимо сдавать через 2-3 недели после удаления опухоли, далее – не реже 1 раза в месяц в течение первого года и не реже 1 раза в 4 месяца в последующие годы.
У беременных женщин с помощью определения уровня ХГЧ можно определить отклонение в развитии плода, угрожающий выкидыш, внематочную беременность, а также вести наблюдение за пациентками после медицинского аборта для исключения осложнений.
Повышенный гонадотропин в сыворотке крови и моче является одним из наиболее достоверных признаков наличия онкологического образования. Определение этого онокмаркера вместе с некоторыми другими (например АФП) широко применяется для диагностики злокачественных процессов и их рецидивов.
Хорионический гонадотропин позволяет выявить онкологическое образование в 100 % случаев раковых заболеваний, возникающих из зародышевых клеток и трофобластом, излечить 95% пациентов без метастазов и 83% пациентов с метастазами.
Состояния, при которых уровень ХГЧ может повышаться и понижаться
О ХГЧ слышал каждый, но что это значит, мало кто понимает. Зачастую считают, что этот показатель определяется только у беременных, однако это не так. Сейчас разберёмся, что это такое, у кого его определяют и с какой целью.

Что собой представляет ХГЧ?
ХГЧ (хорионический гонадотропин человека), ХГ (хорионический гонадотропин) – гликопротеин, с молекулярной массой 36,7 килодальтон.
По своему строению ХГЧ схож с гипофизарными гонадотропинами, например, тиреотропным (ТТГ), фолликулостимулирующим (ФСГ) и лютеинизирующим гормонами (ЛГ). Хорионический гонадотропин так же, как и они, состоит из двух субъединиц (альфа и бета), которые связанны нековалентными связями.
Строение молекулы ХГЧ
Альфа-субъединица схожа у всех четырёх гормонов. Она имеет молекулярную массу 14,5 кДа и кодируется одним геном. Альфа-субъединица состоит из 92 аминокислот. Основное различие между гормонами обеспечивается строением бета-субъединицы.
Бета-субъединица гипофизарных гонадотропинов состоит из 114 – 145 аминокислотных остатков. У ХГЧ она имеет молекулярную массу около 22 кДа. На рисунке 1 представлена схема гомологии (схожести) бета-субъединицы хорионического гонадотропина с ЛГ, ФСГ, ТТГ.
Больше всего бета-субъединица ХГЧ схожа с лютеинизирующим гормоном (75%). Это обусловлено тем, что они взаимодействуют с одним и тем же рецептором. Степень гомологии с фолликулостимулирующим гормоном составляет где-то 35%, а с тиреотропином – 46%.

Под определением хорионического гонадотропина понимают исследования уровня бета-субъединицы или β-ХГЧ, то есть разницы между двумя этими понятиями нет.
Где синтезируется хорионический гонадотропин?
Главным местом синтеза является трофобласт (синцитиальный слой). Попытаемся разобраться, как он образуется с момента зачатия. После оплодотворения яйцеклетки сперматозоидом происходит интенсивное деление клеток. В конце первой недели формируется зародыш, наружная часть которого называется трофобластом. Трофобласт, сливаясь с эндометрием, формирует синцитиотрофобласт. В дальнейшем он разовьётся до хориона, который послужит началом для развития плаценты.
Таким образом, трофобласт обеспечивает прикрепление зародыша к стенке матки (эндометрию) и способствует развитию плаценты, главной функцией которой является обеспечение обмена веществ между матерью и ребёнком.
В беременном состоянии хорион выделяет хорионический гонадотропин. Также важен синтез прогестерона, выделяемый жёлтым телом яичника. Постоянную концентрацию прогестерона поддерживает ХГЧ, затем он начинает выделяться плацентой.
Отсутствие жёлтого тела и как следствие низкое содержания прогестерона может привести к невынашиванию беременности (выкидыши).
Функции, выполняемые ХГЧ
Основная роль ХГЧ заключается в:
- поддержании секреции прогестерона жёлтым телом и плацентой;
- способствует образованию хориона, увеличению количества ворсин, их питание;
- увеличении синтеза гормонов коры надпочечников – адаптация организма к беременности. Глюкокортикоиды подавляют иммунные реакции, направленные на отторжение ребёнка организмом матери, так как плод на 50% состоит из чужеродных антигенов отца;
- способствует выработке половых гормонов (эстрогенов), созреванию мужской половой системы.
Почти всем женщинам известно, что уровень ХГЧ является признаком имеющейся беременности. В основу этого положен механизм действия тест-полосок. Суть заключается в том, что с помощью иммунохроматографического теста можно определить наличие в моче хорионического гонадотропина. Его присутствие говорит о 90% вероятности беременности.

У мужчин и женщин этот гормон может определяться в случае наличия опухоли.
На форумах иногда всплывают сообщения о том, что уровень ХГЧ не показал беременность, однако позднее всё-таки оказалось, что женщина в положении. Такая ситуация могла возникнуть вследствие неправильного введения календаря овуляции, что привело к сдаче анализа в ранний срок.
Правильно высчитать срок беременности может помочь онлайн калькулятор ХГЧ. Вам необходимо ввести день цикла, после овуляции или задержки менструации, также уровень ХГЧ, после чего калькулятор посчитает вам примерный срок в неделях. Исследование уровня хорионического гонадотропина в динамике позволит оценить развитие беременности. Калькулятор сообщит вам о темпах прироста гормона, пояснит, соответствует это норме или нет.
Подготовка к анализу на ХГЧ
Материалом для исследования служит венозная кровь. Подготовка проста и заключается в следующем:
- кровь необходимо сдавать на 4 – 5-й день задержки менструации для более точного результата для подтверждения беременного положения;
- следует воздержаться от физических и эмоциональных перегрузок, и не только потому, что это относится к подготовке к анализу (беременным стоит поберечь свой организм);
- предпочтительнее кровь сдавать натощак, чтобы она была пригодна для исследования;
- категорически запрещено употреблять алкоголь перед любым исследованием и тем более при подозрении на беременность.
Где можно сдать кровь на ХГЧ?
Анализ крови на хорионический гонадотропин можно сдать в рамках программы ОМС в той поликлинике, к которой вы прикреплены (бесплатно). Определением уровня гормона в крови занимаются и частные клиники.
Сколько стоит анализ крови на ХГЧ?
В результате мониторинга цен на разных сайтах популярных медицинских компаний, занимающихся клиническими лабораторными исследованиями, было обнаружено, что в среднем стоимость анализа уровня хорионического гонадотропина (β-ХГЧ) будет около 400 – 600 рублей.
Каковы показания для назначения анализа на ХГЧ?
Анализ крови на ХГЧ назначается с целью:
- подтверждения беременности и оценки её протекания;
- при проведении аборта судят о качестве его проведения;
- выяснить причину отсутствия менструальных кровотечений (беременность опровергнута);
- подозрение на наличие неоплазии яичников и яичек (у мужчин, женщин без беременности);
- диагностика образований, способных выделять этот гормон.
Нормальные показатели ХГЧ
У мужчин и женщин, не находящихся в беременном состоянии, содержание ХГЧ в норме не превышает 5 мЕд/мл или 5 Ед/л. При беременности концентрация ХГЧ растёт с увеличением срока гестации.
В таблице 1 представлены референсные значения уровня ХГЧ в зависимости от срока беременности.
Таблица 1. Недели беременности и уровень ХГЧ
| Срок беременности | Уровень хорионического гонадотропина |
| Первая – вторая недели | 5 — 25 мЕд/мл |
| Третья – четвертая недели | 25 — 156 мЕд/мл |
| Четвертая – пятая недели | 101 — 4870 мЕд/мл |
| Пятая – шестая недели | 1110 — 31500 мЕд/мл |
| Шестая – седьмая недели | 2560 — 82300 мЕд/мл |
| Седьмая – восьмая недели | 23100 — 151000 мЕд/мл |
| Восьмая – девятая недели | 27300 — 233000 мЕд/мл |
| Девятая – тринадцатая недели | 20900 — 291000 мЕд/мл |
| Тринадцатая – восемнадцатая недели | 6140 — 103000 мЕд/мл |
| Восемнадцатая – двадцать третья недели | 4720 — 80100 мЕд/мл |
| Двадцать третья – сорок первая недели | 2700 — 7810 мЕд/мл |
Максимальная концентрация ХГЧ достигает в 11-ю неделю до 291000 мЕд/мл. Затем со второго триместра содержание ХГЧ начинает снижаться, так как часть функций по синтезу гормонов берёт на себя плацента.
При содержании ХГЧ в крови 5 – 25 мЕд/мл не позволяет со 100% уверенностью сказать о наличии беременности. Необходимо повторно сдать кровь через пару дней, где с большей вероятностью будет сделано точное заключение о наличии эмбриона.
При наличии отклонений в развитии беременности уровень ХГЧ будет снижен или повышен. Необходимо тщательное наблюдение за течением беременности.

Низкий уровень ХГЧ
Низкое содержание ХГЧ может говорить о внематочной беременности, угрозе выкидыша, патологии плаценты. Расширенный список причин пониженного уровня хорионического гонадотропина указан в таблице 2.
Таблица 2. Причины низкого содержания ХГЧ
| У беременных женщин | У небеременных женщин и мужчин |
|
|
Низкая концентрация ХГЧ требует внимательного отношения к пациентке, так как это может отразиться на развитии плода, вызывая задержку созревания органов и тканей, имеет отрицательное влияние на плаценту, в результате чего нарушается снабжение плода кислородом и питательными веществами.

Высокий уровень ХГЧ
Высокая концентрация ХГЧ у беременной женщины может говорить о неправильно определённом сроке или количестве эмбрионов, а также о гестозах или диабете. Более подробно о причинах повышения уровня хорионического гонадотропина описано в таблице 3.
Таблица 3. Повышенная концентрация ХГЧ с возможными причинами
| Причины высокого ХГЧ у беременных женщин | Причины высокого ХГЧ у небеременных женщин и мужчин |
|
- Пять дней назад был сделан аборт.
- Приём ХГЧ-содержащих средств.
- Наличие пузырного заноса, хорионкарциномы.
- Злокачественное новообразования яичка (семинома).
- В период менопаузы.
- При нарушении выделительной функции почек вследствие накопления гормона в крови.
Немного о патологии
Хотелось бы немного подробнее остановиться на тех патологических состояниях, на которые может указать изменение уровня хорионического гонадотропина, чтобы донести до пациентов важность определения ХГЧ, если кто-то понял не до конца.
Гестоз
Высокий уровень ХГЧ может указывать на развитие гестоза. Гестоз – состояние, являющееся осложнением беременности, которое сопровождается повышением артериального давления (гипертензия), появлением отёков, протеинурией (белок в моче). Не обязательно все три проявления должны встречаться одновременно. Имеются разные комбинации симптомов гестоза.
Опасность для матери и ребёнка представляют тяжёлые формы гестоза – преэклампсия и эклампсия.
Причиной этого является спазм сосудов вследствие эндотелиальной дисфункции. Снижается объём циркулирующей крови, кровь сгущается, плазма выходит сквозь стенку сосудов в интерстиций. Нарушается функционирование почек, возникает задержка развития плода и гипоксия.
Лечение гестоза проводится стационарно. Терапия симптоматическая, то есть понижают давление, способствуют улучшению микроциркуляции, противосудорожные средства при необходимости.

Пузырный занос
Пузырный занос довольно редкая патология. Из-за несформировавшейся плаценты происходит гибель плода, вместо него образуются кисты, заполненные жидкостью. Причиной этого считают хромосомные нарушения. Выделяют полный и частичный пузырный занос.
- Полный пузырный занос – материнские хромосомы отсутствуют, имеется двойной набор отцовских. Плод погибает, но матка продолжает расти. Для данного вида пузырного заноса характерен высокий риск злокачественного перерождения.
- Частичный пузырный занос – имеется набор материнских и двух отцовских хромосом. Выявляется на 8 – 12-й неделе беременности.
В случае перехода пузырного заноса в стенки матки (инвазивный характер) может возникнуть внутреннее кровотечение.
Лечение заключается в удалении пузырного заноса хирургически путём выскабливания. Оценить качество проведённой терапии поможет уровень ХГЧ. Если гормон не приходит в норму, значит, в матке остались патологические наросты, необходимо повторное выскабливание.
Вакуумная аспирация предлагается тем, кто в дальнейшем желает иметь детей. Материал, полученный в результате удаления пузырного заноса, направляется на исследование для исключения варианта его перерождения.

Хорионэпителиома
Хорионэпителиома – злокачественная опухоль из ворсин хориона. Новообразование повреждает кровеносные сосуды и способствует распространению метастазов. Хорионэпителиома возникает в результате пузырного заноса. Клиническими проявлениями являются маточные кровотечения, повышение температуры тела, боли различной локализации, тошнота, рвота. Лечат хорионэпителиому химиотерапией и противоопухолевыми препаратами. Благоприятный исход имеется в том случае, если опухоль не дала метастазы и поразила только матку.
Злокачественные опухоли яичек
К злокачественным опухолям яичек относятся:
- семинома – наиболее часто встречающееся новообразование, для которого характерно раннее развитие метастазов;
- тератомы;
- хорионкарциномы;
- эмбриональноклеточный рак.
На развитие новообразований оказывает влияние наследственность, крипторхизм (неопущение яичек в мошонку), повышенное количество эстрогенов. Но это не значит, что при наличии данных факторов риска обязательно разовьётся опухоль. Просто необходимо брать во внимание вероятность развития новообразования.
С каждым годом имеются успехи в комбинированном лечении новообразований яичек. У ряда пролеченных наблюдается восстановление репродуктивных функций.

Заключение
Какие выводы можно сделать из всего вышеперечисленного?
- Главная цель исследования уровня ХГЧ – контроль за протеканием беременности. Вовремя обнаруженное отклонение от нормы позволит назначить терапию и не допустить развитие неблагоприятного исхода.
- У мужчин ХГЧ также может быть определён, как и у небеременных женщин, с целью диагностики и оценки эффективности лечения таких заболеваний, как опухоли яичников, яичек, хорионэпителиомы, пузырного заноса.
- Низкое содержание ХГЧ и дополнительные методы исследования (УЗИ) позволят вовремя обнаружить внематочную беременность и исключить возможность неблагоприятного исхода.
Правильное протекание беременности обеспечит будущего малыша здоровьем, поэтому крайне важно относиться к будущим матерям с особой внимательностью.

Мы приложили много усилий, чтобы Вы смогли прочитать эту статью, и будем рады Вашему отзыву в виде оценки. Автору будет приятно видеть, что Вам был интересен этот материал. Спасибо!
Онкомаркер ХГЧ (хорионический гонадотропин человека): зачем и когда назначается, расшифровка результатов
Многие знают, что определение хорионического гонадотропина человека (ХГЧ) в крови используется для ранней диагностики беременности, когда тест-полоска еще не способна определить результат. Но, помимо этого, анализ на ХГЧ применяются при диагностике и мониторинге гестационной трофобластической болезни и герминогенных опухолей. О том, когда врач может назначить данное исследование и как расшифровать результаты, — пойдет речь в этой статье.

Другие названия теста: количественный ХГЧ, β-ХГЧ, общий ХГЧ, общий β-ХГЧ, интактный ХГЧ (англ. Beta hCG, Total hCG, Total beta hCG).
Что исследуется?
Хорионический гонадотропин человека (ХГЧ) — это гормон, состоящий из альфа- и бета-субстанций, который вырабатывается плацентой и обычно выявляется в крови только в период беременности. Однако некоторые аномальные ткани, раки также могут продуцировать ХГЧ, поэтому анализ на ХГЧ может быть использован в качестве индикатора этих опухолей. Исследование подразумевает определение содержания интактного ХГЧ в крови, а иногда отдельно и бета-субъединицы.
Повышенный уровень ХГЧ наблюдается при гестационной трофобластической болезни и некоторых герминогенных опухолях как доброкачественных, так и злокачественных. При этих патологиях тест может использоваться в качестве диагностического инструмента. Помимо этого, с его помощью можно мониторить терапию, а также контролировать течение заболевания.
Гестационная трофобластическая болезнь (ГТБ) — это сборное понятие, включающее группу доброкачественных и злокачественных новообразований, которые развиваются в матке из слоя клеток трофобласта. Трофобласт образует сплошной клеточный покров всего зародышевого комплекса, в дальнейшем формирует эпителиальный покров ворсин хориона, а впоследствии — ворсинок плаценты. Именно его клетки продуцируют хорионический гонадотропин человека. ГТБ обычно возникает в начале беременности после оплодотворения яйцеклетки. Вместо того, чтобы поддерживать рост плода, клетки образуют аномальные тканевые массы. ГТБ возникает примерно в 1 случае на 1000 беременностей. Основными формами ГТБ являются:
- Пузырный занос (молярная беременность) может быть полным (только опухолевая ткань) или частичным (смесью опухолевой и эмбриональной ткани); опухоли обычно доброкачественные, тем не менее, они должны быть удалены хирургическим путем.
- Хариоаденома — среднее состояние между пузырным заносом и хориокарциномой, опухоль врастает в стенку матки; она должна быть удалена.
- Хориокарцинома — редкая злокачественная опухоль, которая может развиться из других форм ГТБ, встречается примерно в 2-7 случаев на 100 000 беременностей; этот тип рака быстро растет и распространяется на другие участки тела.
- Трофобластическая опухоль плацентарной площадки — также встречаются очень редко, формируется на участке прикрепление плаценты к матке. Эта опухоль обычно развивается после нормальной или прерванной беременности, редко дает метастазы.
- Эпителиоидная трофобластическая опухоль — чрезвычайно редкая опухоль, она похожа по своему поведению и природе на хориокарциному, но в настоящее время считается отдельным заболеванием. Может пройти много лет после беременности, прежде чем эта опухоль проявит себя. Как правило, на момент ее выявления уже имеются отдаленные метастазы.
Примечание: современные методики лечения ГТБ позволяют в большинстве случаев добиться полного выздоровления.
Опухоли из зародышевых клеток (герминогенные опухоли) могут быть зло- или доброкачественными, встречаются главным образом в яичниках и яичках, возможна внегонадная их локализация, например, в одной полости.
- Опухоли из зародышевых клеток яичников встречается намного реже, чем эпителиальный рак этого органа и чаще наблюдаются у более молодых женщин.
- Опухоли из зародышевых клеток яичка составляют более 90% случаев рака этого органа (подробнее см. Рак яичка).
Уровни ХГЧ могут быть повышены и при других заболеваниях, например, при раке печени, молочной железы, легких, кожи и желудка. Возможны высокие уровни ХГЧ при циррозе печени, воспалительные заболевания кишечника (язвенном колите и болезни Крона).
Для чего используется исследование?
Количественный анализ хорионического гонадотропина человека (ХГЧ), часто называемый бета-ХГЧ (βhCG), измеряет количество этого гормона, находящегося в крови. Он используется при диагностике гестационной трофобластической болезни (ГТБ), а также совместно с определением АФП (альфа-фетопротеин) и лактатдегидрогеназы его применяют при диагностике опухоли из зародышевых клеток.
Поскольку ХГЧ обычно не выявляется в крови у мужчин и небеременных женщин, он полезен в качестве онкомаркера. Если опухоль или рак продуцируют ХГЧ, то тест может помочь обнаружить и контролировать активность онкопатологии.
Если анализ на ХГЧ используется в качестве опухолевого маркера, в отличие от выявления беременности, важно определять его интактную форму(альфа + бета-субстанции). При некоторых опухолях может быть полезным измерение бета-субстанции. Методики проведения тестов в разных лабораториях могут отличаться. Поэтому очень важно сдавать анализы в одной и той же лаборатории.
Когда назначается исследование?
Количественный тест на ХГЧ может быть назначен при подозрении на гестационную трофобластическую болезнь (ГТБ) или опухоль из зародышевой клетки.
Признаки и симптомы ГТБ могут включать:
- Вагинальное кровотечение во время беременности.
- Усталость, связанная с анемией (если кровопотеря значительна).
- Увеличение живота не соответствующее срокам беременности.
- Преэклампсия на ранних сроках беременности.
- Тошнота или рвота, выраженность которых не соответствует нормально протекающей беременности.
- Положительный тест на беременность (качественная ХГЧ), но на УЗИ плод не определяется.
- Матка, которая остается увеличенной после родов.
Клинические проявления герминогенных опухолей у женщин и мужчин аналогичны симптомом рака яичников и рака яичек соответственно. Если диагностирован один из этих раков, и ХГЧ изначально повышен, то его определение в крови будет проводится через определенные промежутки времени с целью мониторинга эффективности лечения и выявления рецидива.
Что означают результаты?
У мужчин и небеременных женщин ХГЧ обычно не определяется или он выявляется в очень малом количестве.
Если тест используется в качестве опухолевого маркера, повышенный уровень указывает на присутствие герминогенной опухоли (опухоль зародышевой клетки) или на гестационную трофобластическую болезнь (ГТБ).
Высокий уровень встречается как при ГТБ, так и при нормальной беременности. Тем не менее, в начале нормально протекающей беременности ХГЧ повышается с постоянной и предсказуемой скоростью, удвоение показателя происходит примерно каждые 36-48 часов, а для ГТБ характерна непредсказуемость темпов его роста, что, в сочетании с ультразвуковым исследованием, указывает на патологическое течение беременности, требующие вмешательства. Уровни ХГЧ могут быть «чрезмерно» высокими и при нормальной беременности, а также не показывать ожидаемое снижение после беременности или аборта.
Во время лечения ГТБ или герминогенной опухоли падение уровня обычно указывает на то, что заболевание реагирует на терапию (снижение на 50% каждые 1,5 дня). В свою очередь, постоянные или повышающиеся уровни указывают на то, что патологическое состояние прогрессирует. Повышенный ХГЧ после лечения может указывать на рецидив заболевания.
Что еще необходимо знать?
Ложноположительные результаты возможны, если принимаются определенные препараты, таких как противосудорожные, противопаркинсонические, снотворные, а также транквилизаторы. Присутствие их в крови может помешать правильной интерпретации результатов теста. Кроме того, определенные типы антител и фрагменты молекулы ХГЧ, которые присутствуют в крови некоторых людей, также могут повлиять на правильность результата. Как правило, если он вызывает сомнение, определение ХГЧ проводится с помощью других методик.
Редко, но иногда этот онкомаркер используется при диагностике и мониторинге онкологических заболеваний, которые не являются ГТД или герминогенными опухолями.
Можно ли сдать анализ мочи вместо крови?
Если в крови повышен уровень ХГЧ, то он будет высокий и в моче, но результаты не являются взаимозаменяемыми. Кровь является предпочтительным образцом для подтверждения онкологического заболевания.
Можно ли предотвратить гестационную трофобластическую болезнь?
Нет. Патологию нельзя предотвратить, так как она связана с самой беременностью. Это очень редкое заболевание, обычно патология выявляется сразу же после наступления беременности и успешно лечится.
Возможна ли нормальная беременность после ГТБ?
Да, в большинстве случаев, хотя вы подвержены высокому риску повторного пузырного заноса. После лечения ГТБ вам необходимо будет подождать некоторое время, следуя рекомендациям врача, прежде чем снова забеременеть.
Зачем спортсменов проверяют на ХГЧ?
Спортсмены, как любители, так и профессионалы должны периодически проходите допинг-контроль — сдавать анализы на стероиды и другие вещества, повышающие работоспособность. Обычно допинг-контроль осуществляется на протяжении всей их карьеры. Тесты мочи позволяют обнаружить около 200 химических соединений, включая стероиды и другие анаболические вещества, эритропоэтин, а также вещества, которые спортсмен употребляет, чтобы скрыть незаконное использование допинга. Это так называемые маскирующие агенты, то есть, позволяющее получить ложноотрицательные результаты допинг-тестов.
Некоторые спортсмены, которые используют в качестве допинга стероиды, принимают бета-ХГЧ, чтобы уменьшить побочные эффекты их использования. Поэтому иногда спортсменов проверяют на ХГЧ, чтобы подтвердить использование стероидов.
Хгч продуцирующие опухоли
Хорионический гонадотропин человека (ХГЧ) — это не только всем известный показатель наличия беременности, но и онкомаркер. Однако функция его двоякая: если ранее при наличии опухоли считалось, что повышение уровня ХГЧ в сыворотке крови достоверно указывает на плохой клинический прогноз, то сегодня на основе этого белка создаются вакцины против рака. В чем же причина такого изменения отношения к ХГЧ?
Хорионический гонадотропин человека — это гликопротеин, в норме продуцируемый клетками синцитиотрофобласта здоровых беременных женщин. Его выработка начинается в первые 3-5 дней после оплодотворения, и уровень ХГЧ в сыворотке крови женщины постепенно нарастает, достигая своего пика к 3 месяцу беременности.
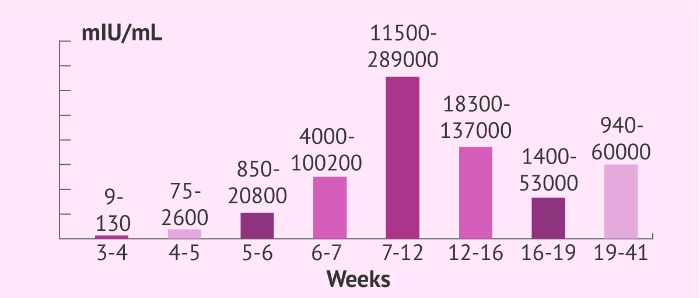
Рисунок 1 ❘ Динамика уровня бета-ХГЧ в сыворотке крови беременных женщин в соответствии со сроком беременности.
В строении ХГЧ выделяют альфа- и бета-субъединицы, связанные нековалентной связью. Альфа-субъединица по химическому строению аналогична гипофизарным гонадотропным гормонам, что делает невозможным использование ее как онкомаркера. Бета-субъединица, напротив, является строго специфичной и потому используется для диагностики беременности, многих акушерских и гинекологических патологий (например, пузырного заноса), а также нетрофобластических злокачественных опухолей. Так, бета-ХГЧ может обнаруживаться в сыворотке крови мужчин и небеременных женщин в концентрации выше 5 мЕд/мл при раке яичка и яичника, гепатоцеллюлярной карциноме, остеосаркоме, раке молочной железы и прямой кишки.
При беременности ХГЧ участвует в имплантации зародыша. В случае экспрессии в тканях нетрофобластических злокачественных опухолей ХГЧ имеет независимые функции, которые на сегодняшний день изучены не полностью. Исследования показывают, что бета-субъединица белка способна ингибировать апоптоз или стимулировать рост опухолевых клеток, и повышение ее уровня в сыворотке крови коррелирует с растущей агрессивностью опухоли. Например, при остеосаркоме высокий уровень ХГЧ в сыворотке крови ассоциирован с наличием опухоли, слабо реагирующей на неоадъювантную терапию. Однако прежде всего в современной диагностике ХГЧ используется как маркер рака яичника. Присутствие ХГЧ в сыворотке крови обнаруживается у 27% пациенток с доброкачественными опухолями и 67% пациенток с раком яичника. В ткани опухоли ХГЧ выделяют в 68% случаев вне зависимости от ее гистологического типа. При этом важно отметить, что встречаются методы определения в сыворотке крови не самого бета-ХГЧ, а его гипергликозилированных фракций. Показатели уровня белка в целом, его бета-субъединицы или гипергликозилированных фракций являются взаимозаменяемыми в диагностике злокачественных новообразований.
Среди всех функций ХГЧ в онкогенезе наиболее интересна следующая. Установлено участие этого белка в процессе васкулогенной мимикрии в ткани опухоли яичника. Васкулогенная мимикрия — это способность опухолевых клеток приобретать фенотип эндотелиоцитов и формировать аналогичные сосудам каналы для обеспечения кровоснабжения опухоли. Способность опухоли к васкулогенной мимикрии коррелирует с возрастающим риском метастазирования и неблагоприятным клиническим прогнозом. На основании этих данных была начата разработка препаратов на основе моноклональных антител, связывающих ХГЧ, а также вакцин, снижающих его выработку опухолевыми клетками in vitro.
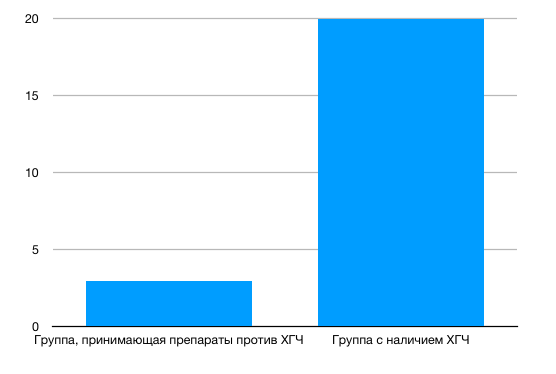
Рисунок 2 ❘ Среднее количество каналов, образованных по типу васкулогенной мимикрии, в ткани опухоли пациентов без ХГЧ и с обнаруженным ХГЧ в сыворотке крови.
Известно, что бета-ХГЧ участвует и в формировании опухолей молочной железы, однако его роль в онкогенезе считается противоречивой: одни исследования причисляют ему антионкогенные функции, другие называют его скорее проонкогенным фактором. В 2017 году было впервые установлено, что экспрессия ХГЧ связана с состоянием гена BRCA1, и повышение продукции белка наблюдается именно у пациентов с наличием мутации в этом гене. В ткани такой опухоли бета-ХГЧ запускает процессы миграции и инвазии клеток. Кроме того, хорионический гонадотропин принадлежит к семейству белков, способных формировать так называемый структурный “цистиновый узел”. Схожую структуру имеет трансформирующий фактор роста, участвующий в опухолевой прогрессии. Было установлено, что ХГЧ способен связываться с рецепторами к ТФР-бета и фосфорилировать их, что запускает пролиферацию клеток с дефектами гена BRCA1. Прерывание взаимодействия бета-ХГЧ и рецепторов к ТФР-бета может стать эффективной стратегией терапии рака молочной железы.
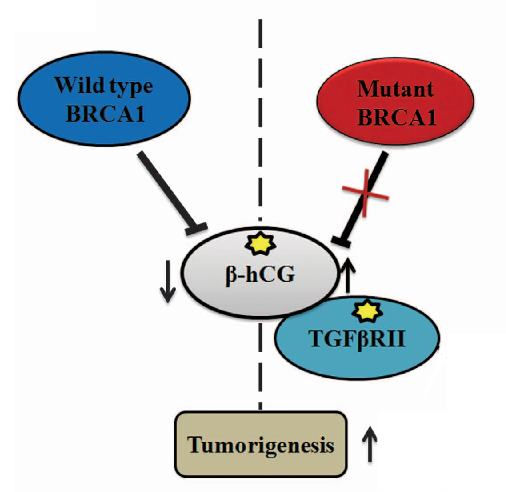
Рисунок 3 ❘ Упрощенная схема взаимодействия мутантного BRCA1 и бета-ХГЧ в формировании опухоли молочной железы.
Наиболее интересен тот факт, что встречаются и прямо противоположные данные в отношении роли ХГЧ в развитии рака молочной железы. Так, предположительно этот белок является защитным агентом против данного типа опухолей, а вакцина на основе бета-субъединицы ХГЧ не так давно показала свою эффективность против рака молочных желез у мышей. Известно, что беременность является защитным фактором против рака молочной железы. Именно ХГЧ предположительно формирует антионкогенный эффект состояния беременности, изменяя геном клеток молочных желез и тем самым делая их более устойчивыми к опухолевой трансформации. Также ХГЧ беременной женщины оказывает проапоптотический эффект, снижая выработку белков-маркеров пролиферации и повышая активность факторов апоптоза (в том числе широко известного p53).
Таким образом, плацентарный ХГЧ и эктопически экспрессируемый белок имеют противоположную роль в онкогенезе, что представляет интерес для исследователей в разных направлениях научной деятельности. Полученные знания имеют и высокую практическую ценность, ведь в настоящее время имитация беременности путем введения ХГЧ предложена как вариант предотвращения рака молочной железы, а управление продукцией бета-ХГЧ в опухолевых клетках может стать эффективным направлением таргетной терапии других опухолей.
Источники:
1. An HCG-rich microenvironment contributes to ovarian cancer cell differentiation into endothelioid cells in a three-dimensional culture system. / Min Su, Chao Fan, Sainan Gao [et al] // Oncol Rep. – 2015. – Vol. 34, №5. – p. 2395-2402.
2. Does hCG or hCG-beta play a role in cancer cell biology? / R. K. IIes, P. J. Delves, S. A. Butler. // Mol Cell Endocrinol. – 2010. – Vol. 329, №1-2. – p. 62-70.
3. Ectopic production of beta-hCG by osteosarcoma: a case report and review of the literature. / Oshrine BR, Sullivan LM, Balamuth NJ // J Pediatr Hematol Oncol. – 2014. – Vol. 36, №3. – p. 202-206.
4. A preliminary investigation of beta-hCG expression in patients with osteosarcoma. / Masrouha KZ, Khattab R, Tawil A [et al] // J Bone Joint Surg Br. – 2012. – Vol. 94, №3. – p. 419-424.
5. Hyperglycosylated hCG, hCG-beta and Hyperglycosylated hCG-beta: interchangeable cancer promoters. / Cole LA, Butler S. // Mol Cell Endocrinol. – 2012. – Vol. 349, №2. – p. 232-238.
6. Human Chorionic Gonadotropin and Breast Cancer. / Susanne Schuler-Toprak, Oliver Treeck, Olaf Ortmann. / Int J Mol Sci. – 2017. – Vol. 18, №7. – p. 1587.
7. Human chorionic gonadotropin and its relation to grade, stage and patient survival in ovarian cancer. / Lenhard M, Tsvilina A, Schumacher L [et al] // BMC Cancer. – 2012. – Vol. 12, №2.
8. BRCA1 regulation on beta-hCG: a mechanism for tumorigenicity in BRCA1 defective breast cancer. / S K Sengodan, R Nadhan, R S Nair [et al] // Nat Oncogen. – 2017. – Vol. 6. – p. 376.
Что показывает анализ крови на ХГЧ и как подготовиться к исследованию
ХГЧ (хорионический гонадотропин человека) часто называют «гормоном беременности», поскольку именно он отвечает за регуляцию гормональных процессов в женском организме в период вынашивания плода. Однако анализ крови на ХГЧ назначают не только женщинам, но и мужчинам. О том, кому необходимо исследование и как расшифровать результаты, — пойдет речь в этой статье.
ХГЧ: роль в организме и суть анализа
Хорионический гонадотропин человека — гормон, который вырабатывается компонентом оплодотворенной яйцеклетки — синцитиотрофобластом. После имплантации к стенке матки ХГЧ стимулирует развитие плаценты. Но следует знать, что этот гормон вырабатывается и при раковых заболеваниях (и у женщин, и у мужчин), поэтому анализ на ХГЧ используют также для диагностики онкологии. Вопрос о том, является ХГЧ причиной или следствием рака, — остается открытым. Поэтому в некоторых зарубежных странах запрещена безрецептурная продажа гомеопатических и диетических препаратов с содержанием ХГЧ.
ХГЧ состоит из альфа- (a) и бета- (b) единиц. Первая идентична лютеинизирующему и тиреотропному гормону; вторая является уникальной для хорионического гонадотропина человека. Поэтому именно ее показатели имеют определяющее значение в лабораторном анализе. В плазме крови бета-единица выявляется примерно на 6–8 день после того, как произошло оплодотворение. Спустя 7 дней после родов хорионический гонадотропин уже не должен обнаруживаться в моче и крови.
ХГЧ выполняет следующие функции:
- способствует сохранению желтого тела и ускоряет выработку прогестерона и эстрогена — на первых неделях беременности;
- у плода стимулирует работу половых желез и надпочечников;
- готовит иммунитет матери к принятию плода;
- стимулирует клетки Лейдига, вырабатывающие тестостерон у эмбрионов мужского пола.
Повышение ХГЧ может указывать на беременность, однако рост концентрации гормона свидетельствует также об аномалии плода, сахарном диабете у матери или раке. Сравнивая показатели уровня гормона на разных сроках беременности, врач может выявить внематочную беременность.
У мужчин повышение уровня этого гормона может быть спровоцировано опухолевыми заболеваниями, в том числе тератомой и семиномой яичка. Понижение уровня ХГЧ также чревато последствиями. Его показатели отличаются у разных категорий пациентов.
Типы анализов на ХГЧ
В медицинской практике известны два анализа на ХГЧ: определение общего ХГЧ и определение свободного бета-ХГЧ. Они используются в разных целях.
Общий ХГЧ
Анализ крови на общий ХГЧ используется для ранней диагностики беременности, когда тест-полоска еще не способна определить результат. При отсутствии патологий уровень гормона в первые недели беременности удваивается каждые 2 дня, максимум достигается к 10–11 неделе. Затем концентрация постепенно снижается.
Во втором триместре беременности анализ на общий ХГЧ назначается в составе пренатального скрининга — так называемого тройного или четверного теста.
Свободный b-ХГЧ
Такой анализ является показательным при диагностике трофобластных (пузырный занос, хориокарцинома) и тестикулярных (онкология яичек) новообразований.
Кроме того, он используется при скрининге первого и второго триместров беременности с целью оценки риска наличия синдрома Дауна и синдрома Эдвардса у плода. Положительный результат анализа ставит женщину в группу риска, но не является стопроцентным показателем развития хромосомных аномалий плода. Беременным советуют сдавать кровь на свободный бета-ХГЧ на 8–13 и на 15–20 неделях. Возраст старше 35-ти лет, болезнь Дауна в анамнезе, врожденные пороки и наследственные болезни у ближайших родственников, облучение радиацией — становятся особыми показаниями для назначения исследования.
Когда можно сдавать кровь на анализ ХГЧ
Анализ крови на ХГЧ проводится не только у женщин, но и у мужчин. Как мы уже писали выше, уровень хорионического гонадотропина человека в крови необходимо знать при диагностике опухолей яичек. Нормальные показатели у мужчин — менее 5 мЕд/мл.
Причин для исследования крови на ХГЧ у женщин гораздо больше. Во-первых, это подозрение на беременность. Во-вторых, длительная задержка менструации, которая может быть последствием дисфункции яичников, стресса, интоксикации, инфекции и других неприятных состояний. В-третьих, подозрение на трофобластические опухоли или наблюдение после перенесенного заболевания такого рода.
У женщин, вынашивающих ребенка, анализ проводится для динамического наблюдения за течением беременности и во время пренатальной диагностики, а также при подозрении на внематочную беременность.
Как сдавать кровь на анализ ХГЧ
Как общий, так и свободный b-ХГЧ определяется при анализе венозной крови. Эксперты советуют сдавать кровь утром натощак. Последний прием пищи рекомендован за 8–10 часов до сдачи биоматериала. Если пациент принимает какие-либо медицинские препараты, следует заранее сообщить об этом врачу. На уровень ХГЧ могут повлиять лишь лекарства, которые содержат этот гормон. В том числе они применяются в лечении бесплодия для стимуляции овуляции. Специалисты утверждают, что ни одно другое лекарственное средство исказить результат анализа крови на хорионический гормон человека не может.
Для уточнения срока беременности лабораторное исследование следует проводить не раньше 4–5 дня задержки менструации, для уточнения результатов можно повторить тест через 2–3 дня. Во втором триместре рекомендуется сдавать анализ на ХГЧ для выявления патологии плода.
Анализ крови на ХГЧ проводится и после аборта или медицинского выскабливания. Если плодное яйцо удалено не полностью, уровень исследуемого вещества будет выше нормального. Для исключения ложноположительного результата тест следует проводить спустя 1–2 дня после операции.
Получение результатов
Исследование крови на ХГЧ проводится методом иммуноферментного анализа сыворотки крови.
Сроки выполнения анализов зависят от конкретного центра, в котором выполняется тест. Как правило, в каждой лаборатории можно заказать экспресс-тест, который будет готов через час–два. Некоторые филиалы исследовательских учреждений отправляют лабораторные материалы в другой регион, вследствие чего результаты клиент сможет узнать не ранее чем через сутки.
Результаты можно получить как лично, так и по Интернету, большинство лабораторий предоставляют своим посетителям доступ в «Личный кабинет» на сайте учреждения, где хранятся результаты всех проведенных в этом заведении исследований. Некоторые центры отправляют итоги экспертизы на электронную почту клиента с предупреждением о конфиденциальности информации и неразглашении ее посторонним лицам.
Единицы измерения ХГЧ — мЕд/мл. Однако некоторые лаборатории могут использовать и альтернативные единицы — Ед/л. Показатели, которые считаются нормой, также могут отличаться в разных лабораториях, поэтому врачи рекомендуют сдавать анализ повторно в одном и том же месте.
Как расшифровать анализ крови на ХГЧ
Для разных категорий пациентов нормальный уровень ХГЧ индивидуален. Самостоятельно расшифровывать анализ можно, но достоверность ваших выводов будет сомнительной. В любом случае диагностировать результат должен специалист.
Рассмотрим нормативные значения:
- У здоровых мужчин уровень ХГЧ в крови должен находиться в интервале до 2,5 мЕд/мл.
- У здоровых женщин, не вынашивающих ребенка, результат анализа покажет от 0 до 5 мЕд/мл.
- Для беременных результат исследования хорионического гонадотропина человека меняется буквально каждые 1–2 недели:
- на 1-й неделе он колеблется в диапазоне от 20 до 150 мЕд/мл;
- на 2-3-й неделе вырастает от 100 до 4870 мЕд/мл;
- на 4-й неделе результат составляет примерно 2500–82 000 мЕд/мл;
- на 5-й неделе уровень ХГЧ в крови может достичь 151 000 мЕд/мл;
- на 6-й неделе развития плода верхний показатель может составить 233 000 мЕд/мл;
- показатели 7–10 недель — 20 900–291 000 мЕд/мл;
- к 16-й неделе уровень ХГЧ падает и может составлять от 6150 до 103 000 мЕд/мл;
- к 20-й неделе в анализе беременной женщины показатели ХГЧ составляют от 4730 до 80 000 мЕд/мл;
- с 21 по 39 неделю интервал показателей — 2700–78 000 мЕд/мл.
Следует учитывать, что нормы исследовательских центров могут отличаться. Поэтому за расшифровкой результатов анализа рекомендуется обращаться в ту же лабораторию, где проводилось обследование.
Повышенные показатели ХГЧ в крови мужчины и небеременных женщин могут говорить о наличии онкологических заболеваний кишечника, легких, почек, матки или яичек и других органов. Кроме того, высокий уровень хорионического гонадотропина человека фиксируется в течение 4–5 дней после аборта и вследствие приема препаратов, содержащих ХГЧ.
У вынашивающих ребенка заметно повышается уровень ХГЧ в результате:
- многоплодной беременности;
- сахарного диабета;
- раннего токсикоза, гестоза;
- пролонгированной беременности;
- хромосомных аномалий плода;
- приема синтетических гестагенов — препаратов, восполняющих в организме уровень главного женского гормона — прогестерона.
Низкие показатели уровня ХГЧ у беременных требуют внимательного отношения и незамедлительного обращения к специалистам. Снижение уровня более чем на 50% от нормы может быть свидетельством внематочной или неразвивающейся беременности, угрозы прерывания, плацентарной недостаточности, истинного перенашивания беременности и внутриутробной гибели плода на поздних сроках.
Насколько точен анализ крови на ХГЧ
Анализ крови на ХГЧ является наиболее достоверным методом определения беременности. Однако в любом исследовании не исключены ошибки, которые допускаются вследствие человеческого фактора — нарушении правил пациентом или лаборантом. Женщины, которые на протяжении долгого времени имели проблемы с деторождением или принимали ряд препаратов, должны сообщить об этом перед проведением исследования. Дело в том, что подобные факторы могут исказить результат анализа.
По статистике у 2% девушек, сдающих кровь на ХГЧ, исследование показывает ложноположительный результат беременности. Это может быть свидетельством гормонального сбоя или наличия ракового заболевания. Бывает и так, что во время подтвержденной беременности анализ показывает отрицательный результат. Это происходит, если овуляция или имплантация плода произошли позже обычного или в случае внематочной беременности.
Современные лабораторные исследования поражают достоверностью и точностью результатов. Им подвластны определение и контроль даже самой минимальной концентрации важных веществ и соединений в организме человека. Показатели ХГЧ и правильная их расшифровка — во многих случаях вопрос жизни и смерти. Независимо от результата анализа следует помнить, что верную расшифровку ХГЧ может произвести только квалифицированный врач, который сделает заключение в комплексе с информацией, полученной по итогам других методов обследования.

Тесты на беременность, которые можно купить в аптеке, достаточно достоверны — в более чем 90% случаев показывают правильный результат. Если после проведения теста у вас остались сомнения — вы можете купить еще несколько тестов других производителей (продукция, выпускаемая под разными брендами, обладает разной чувствительностью). Но лучше всего не тратить понапрасну ни деньги, ни время и сдать кровь на анализ.
Значение опухолевых маркеров в клинике герминогенных опухолей яичка
З.Г.Кадагидзе, В.М.Шелепова, А.В.Соколов
Российский онкологический научный центр им. Н.Н.Блохина РАМН, Москва
Общеизвестно, что за последние 15 лет достигнуты большие успехи в лечении трофобластических неоплазм и герминогенных опухолей. В онкологических центрах, специализирующихся на лечении этих заболеваний, частота излеченности больных превышает 90%. Главными причинами наблюдаемого значительного прогресса являются, наряду с внедрением новых лекарств — цисплатина, VP16-213 и др., — также и рациональное использование опухолевых маркёров.
Наиболее информативными при герминогенных опухолях считаются a-фетопротеин (АФП) и хорионический гонадотропин человека, b-субъединица (b-ХГЧ).
АФП представляет собой гликопротеин с молекулярной массой 70 кД. Он является физиологическим продуктом желточного мешка, печени и желудочно-кишечного тракта плода. Повышенный уровень сывороточного АФП у пациентов с герминогенными опухолями яичка был впервые обнаружен Абелевым в 1997 г. В герминогенных опухолях АФП продуцируется элементами эндодермального синуса (желточного мешка). У детей старше года, как и у взрослых, сывороточный АФП имеет верхнюю границу нормы 15 нг/мл (
10kE/л). Его концентрация может быть повышенной при доброкачественных заболеваниях печени и некоторых злокачественных новообразованиях. Наиболее часто повышенные уровни наблюдаются при герминогенных опухолях и гепатоклеточной карциноме, но иногда также — при раке желудка, кишечника, желчного пузыря, поджелудочной железы и лёгких (приблизительно у 20% пациентов). Полупериод жизни сывороточного АФП после орхэктомии составляет 4-5 дней.
ХГЧ относится к гликопротеиновым гормонам, м.м. 46 kД. Он состоит из двух нековалентно связанных субъединиц — a и b, из которых последняя определяет его уникальные иммунологические свойства. Физиологически ХГЧ продуцируется в синцитиотрофобластах плаценты. В герминомах он образуется трофобластическими структурами или синцитиотрофобластическими гигантскими клетками. Концентрация сывороточного ХГЧ находится в прямой зависимости от массы опухоли и может достигать нескольких миллионов E/л при распространённом заболевании. Подсчитано, что концентрация 1 Е/л соответствует приблизительно 10000 опухолевых клеток. Некоторые нетрофобластические опухоли также синтезируют ХГЧ. Очень высокие концентрации сывороточного ХГЧ наблюдаются при пузырных заносах («молярная» беременность) и хорионкарциномах (97%). Уровни сывороточного ХГЧ могут быть повышенными при аденокарциномах поджелудочной железы и островково-клеточных опухолях, опухолях толстой и тонкой кишки, печени, желудка, лёгких, яичника, молочной железы и почек. При использовании ХГЧ в качестве опухолевого маркёра весьма желательно определение его свободной b-субъединицы (b-ХГЧ), поскольку большинство герминогенных опухолей способны продуцировать лишь b-ХГЧ. Область нормальных значений сывороточного ХГЧ для мужчин и женщин в пре-менопаузе — приблизительно 5 Е/л, для женщин в постменопаузе — до 10 Е/л. Полупериод жизни интактного сывороточного ХГЧ составляет 16-24 ч.
В клинической практике эти маркёры используются для диагностики, мониторинга и прогноза герминогенных опухолей яичка.
Роль АФП и b-ХГЧ в диагностике.
Скрининг на наличие герминогенных опухолей по биохимическим тестам в общей популяции проводить не рекомендуется. При клиническом подозрении герминогенной опухоли (основанном на данных пальпации и УЗИ яичка) определение опухолевых маркёров может быть иногда полезным в дифференциальной диагностике злокачественной опухоли и эпидидимитов у пациентов с безболезненным опуханием одного из яичек. Использование маркёров в дополнение к рентгенологическому и ультразвуковому исследованию брюшной полости повышает диагностическую чувствительность в отношении как гонадных, так и внегонадных (медиастинальных, забрюшинных, центральной нервной системы) герминогенных опухолей.
Связь маркёров с патологией. Проблема диагностики рака яичка состояла, прежде всего, в дифференциации семиномных и несеминомных герминогенных опухолей. В настоящее время эта проблема в большой мере решена благодаря использованию АФП и b-ХГЧ. (таблица 1).
Таблица 1.
Наличие АФП и b-ХГЧ в сыворотке в зависимости от гистологического строения опухоли.
| Гистологическое строение опухоли | АФП | b -ХГЧ |
| Семинома чистого типа | — | — |
| Эмбриональный рак чистого типа | — | — |
| Тератомы незрелые | — | — |
| Тератокарциномы | + | + |
| Опухоли желточного мешка (из эндодермального синуса) | + | — |
| Желточный мешок + другие | + | +/- |
| Хорионкарциномы | — | + |
| Хорионкарциномы + другие | +/- | + |
| Низкодифференцированный рак | +/- | +/- |
Как можно видеть из представленных данных, все больные с герминогенными опухолями яичка в зависимости от наличия маркёров могут быть разделены на две группы. К первой группе (
20 %) относятся больные, опухоли которых не продуцируют АФП и ХГЧ. Это семиномы (типичные, анапластические и сперматозоидные), зрелые тератомы и так называемые эмбриональные карциномы чистого типа. Если они содержат гигантские клетки синцитиотрофобласта, может выявляться небольшое количество ХГЧ, концентрация которого редко превышает 75 мМЕ/мл в основном у больных с III стадией заболевания. Таким образом, отсутствие маркёров не исключает наличия опухолевого процесса. Ко второй группе (около 80% больных с герминогенными опухолями) относятся «маркёрные» больные. Это пациенты с опухолями желточного мешка, продуцирующими АФП, хорионкарциномами, продуцирующими ХГЧ, и со смешанными опухолями (эмбриональные карциномы или тератокарциномы с наличием других гистологических элементов), продуцирующими обычно АФП и/или ХГЧ. Данные по чувствительности маркёров в соответствии с гистологическим типом опухоли приведены в таблице 2.
Таблица 2
Частота герминогенных опухолей яичка с АФП>10kE/л, b-ХГЧ>5E/л.
| Гистологическое строение | АФП+ | ХГЧ+ |
| Несеминомные опухоли | ||
|---|---|---|
| Низко- и средне-дифференцированная злокачественная тератома | 70-72% | 55-60% |
| Зрелая тератома | 0% | 0% |
| Желточный мешок | 64% | 0% |
| Трофобластическая дифференцировка | 0% | 100% |
| Смешанные опухоли | 50-80% | 50-60% |
| Все | 60-80% | 40-60% |
| Семинома | ||
| Семинома | 0% | 15-20% |
Поскольку подходы к лечению семиномных и несеминомных герминогенных опухолей различаются, определение АФП и b-ХГЧ имеет очень важное практическое значение, и часто эти маркёры оказываются более информативными, чем патоморфологическое заключение. Так, по совокупным литературным данным, высокие уровни ХГЧ позволяют распознать трофобластические структуры, нераспознанные в рутинном патогистологическом рапорте, примерно в 10% семином и приблизительно в 30% несеминомных герминогенных опухолей. Практически не вызывает сомнения, что, если у пациентов с семиномой уровень ХГЧ повышен, то в опухоли имеют место быть несеминомные элементы, которые влияют на эффективность лечения и выживаемость.
Использование маркёров для стадирования. При клинической стадии I показано оперативное лечение. Второе определение маркёров проводят через 5-6 дней после операции, чтобы вычислить полупериод жизни соответствующего маркёра. Таким образом, установленная клинически стадия заболевания может быть подтверждена ретроспективно, если концентрация маркёра снижается в соответствии с полупериодом его жизни. До 1997 г. клиническое и патологическое стадирование герминогенных опухолей основывалось только на распространённости заболевания в соответствии с системой ТNM. Следовательно, для стадирования первичной опухоли необходимо было проведение орхэктомии, для классификации N и М — радиографическое исследование грудной клетки, брюшной полости и таза. Определение исходных (до лечения) уровней АФП, ХГЧ и ЛДГ было рекомендовано для клинической практики на основании результатов, полученных в ходе обширного исследования, включавшего 5000 пациентов с герминогенными опухолями и проводившегося под эгидой Международной Группы по изучению герминогенных опухолей — IGCTCG (The International Germ Cell Tumour Collaborative Group). Эти маркёры официально не включены в качестве обязательных в Международную систему по стадированию герминогенных опухолей, но благодаря их определению до и сразу же после орхэктомии, частоту ошибок клинического стадирования удаётся снизить с 50% до менее чем 15%.
Роль маркёров в лечении и наблюдении за больными.
Рациональное использование маркёров находится в соответствии со стадией заболевания.
Стадии 1А и 1В. После проведения паховой орхэктомии более предпочтительным, чем диссекция забрюшинных лимфоузлов, является наблюдение за больным. Наряду с клиническим обследованием и рентгенологическим исследованием органов грудной клетки должно проводиться рутинное определение опухолевых маркёров: ежемесячно в течение первого года после орхэктомии, а затем каждые 6 месяцев во второй и третий годы. Если после орхэктомии уровни АФП и b-ХГЧ остаются повышенными, и полупериод жизни маркёров увеличен, то, несмотря на то, что, по данным компьютерной томографии, остаточная опухоль не обнаруживается, существует высокая вероятность отдалённых метастазов; при этом системная химиотерапия будет предпочтительнее по сравнению с диссекцией забрюшинных лимфоузлов.
Стадия II. После удаления забрюшинных лимфоузлов и либо а) проведения 3-4 циклов химиотерапии, либо б) проведения 2-х циклов адъювантной химиотерапии непосредственно после диссекции — в обоих этих случаях мониторинг больных должен включать, наряду с физикальным и рентгенологическим обследованием, определение опухолевых маркёров: ежемесячно в течение первого года, каждые 3 месяца на протяжении второго года и 1 раз в 6 месяцев на протяжении 3-го года.
Распространённые стадии II и III. Скорость снижения опухолевых маркёров после химиотерапии прогнозирует ответ на лечение. Устойчивое повышение уровня маркёра или удлинение полупериода его жизни в первые 6 недель после специфической химиотерапии указывают на резистентность опухоли и плохой прогноз. Пациенты с остаточной опухолевой массой после проведения химиотерапии могут быть подвергнуты оперативному лечению. Однако, в тех случаях, когда уровни маркёров устойчиво повышаются, пациенты чаще всего оказываются иноперабельными, и вместо операции им показана химиотерапия.
Несеминомные герминогенные опухоли содержат различные типы клеток. Помимо этого, опухоль, которая синтезировала оба маркёра, в ходе лечения может переключиться на продукцию лишь одного из них. Случается, что безмаркёрная до лечения опухоль при рецидиве начинает продуцировать один или оба маркёра в больших количествах. Поэтому необходимо вести мониторинг с использованием обоих маркёров — как АФП, так и b-ХГЧ. Следует также учитывать, что в опухолях со смешанным типом клеток снижение концентрации АФП и b- ХГЧ после резекции отражает соответствующее уменьшение опухолевой массы, в то время как снижение уровней маркёров после химиотерапии отражает лишь поведение маркёр-положительного типа клеток.
После полного удаления опухоли уровни маркёров должны снижаться до нормальных значений в соответствии с их полупериодами жизни: для АФП 1000 кЕ/л, ХГЧ >10000 МЕ/л, опухолевые массы в средостении более 5 см в диаметре и 20 и более метастатических узлов в лёгких. IGCTCG предлагает использовать систему стадирования для метастатических герминогенных опухолей (как семиномных, так и несеминомных), основанную на факторах прогноза. Это позволяет подразделить опухоли на 3 группы — с хорошим, средним и плохим прогнозом — в зависимости от концентрации опухолевых маркёров, как показано в табл.3.
Таблица 3.
Вклад опухолевых маркёров в классификацию прогноза метастатических герминогенных опухолей
| Концентрация опухолевых маркёров | ||
| Группа прогноза1 | АФП (кЕ/л) ХГЧ (Е/л) ЛДГ (х RR)2 | |
| Хороший (S1) | 10 000 >50 000 >10 x (RR) | |
1) — S, сывороточный уровень маркёра
2) — концентрация ЛДГ выражена как произведение соответствующего значения на верхний предел референс-границы (RR- Reference Range).
Предлагаемая система учитывает также расположение опухоли (яичко, забрюшинная область, средостение) и наличие или отсутствие внелёгочных висцеральных метастазов. Для этих трёх прогностических групп частота безрецидивного периода и средней выживаемости составляет, соответственно: для S1 — 89% и 92%, для S2 — 75% и 80%, для S3 — 41% и 48%.
При лечебном мониторинге рекомендуется определять полупериод жизни АФП и ХГЧ; нормализация обоих маркёров (АФП за 5 дней, ХГЧ за 1-2 дня) предполагает благоприятный прогноз. У пациентов с полупериодом жизни АФП более 7 дней и/или ХГЧ более 3 дней частота выживаемости значительно ниже. Система прогноза распространённых герминогенных опухолей была значительно улучшена за счёт использования разработанных в Великобритании United Kingdom Medical Research Council — MRC — комбинированных прогностических критериев, включающих анализ полупериода жизни маркёров (табл. 4). На основании этого пациенты также подразделяются на 3 группы риска.
Таблица 4.
Прогностическая классификация для метастазирующих герминогенных опухолей, основанная на прогностических критериях UK MRC и измерении опухолевых маркёров.
| Классификация на основе | 10-летняя выживаемость | ||
| Группа прогноза | Прогностические критерии UK MRC | Полупериод жизни маркёров | |
| Хороший | Good risk | Нормальный («good») | 96% |
| Средний | Good risk | Нормальный полупериод жизни («good») | 64% |
| Poor risk | Увеличенный полупериод жизни («bad») | ||
| Плохой | Poor risk | Увеличенный («bad») | 28% |
Итак, герминогенные опухоли являются уникальным примером интеграции опухолевых маркёров в диагностику, стадирование и мониторинг терапии. При дифференциальной диагностике чистых семином и опухолей с трофобластическими элементами повышенные уровни ХГЧ более доказательны, чем гистологическое заключение, что имеет значение для выбора терапии. Помимо этого, определение опухолевых маркёров позволяет более аккуратно поставить стадию заболевания. Кинетика маркёров на протяжении первых 6 недель химиотерапии обеспечивает важную прогностическую информацию. У пациентов в ремиссии повышение уровней АФП и ХГЧ может прогнозировать рецидив за несколько месяцев до его клинического диагностирования. Определение маркёров показано при оценке ответа на терапию, а их нормализация является предпосылкой для успешной операции после воздействия химиотерапии.