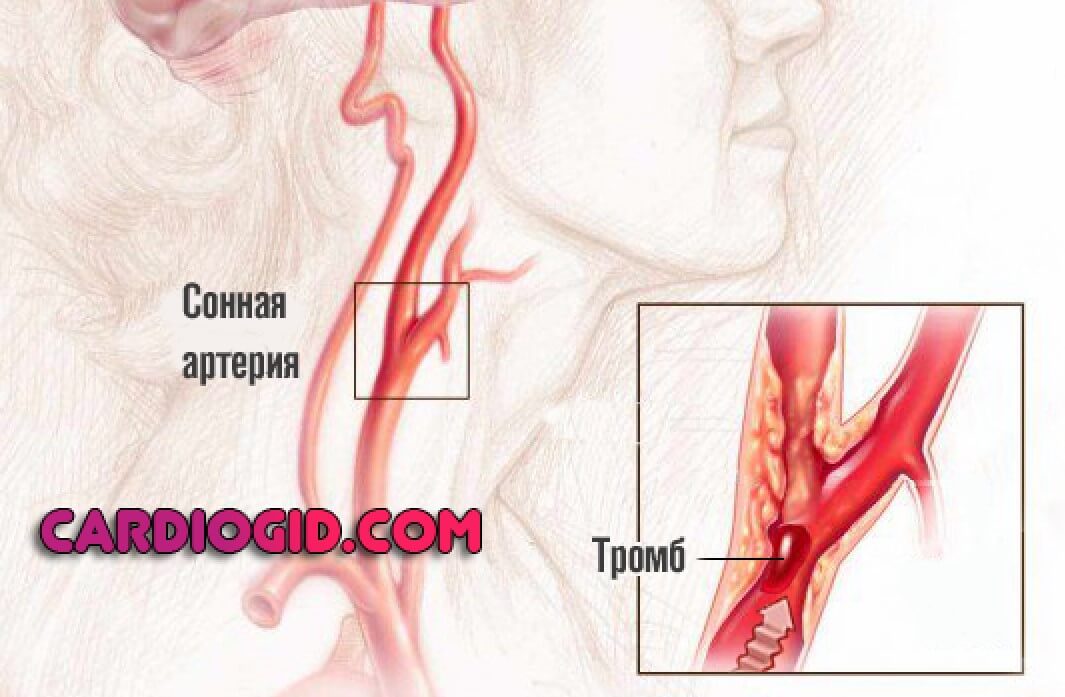
Отек мозга лечение препараты
Данный вид медицинской помощи должен осуществляться в отделениях реанимации и интенсивной терапии и быть построен на нижеприведенных принципах лечения отека головного мозга (Ш. Ш. Шамансуров и др., 1995).
Коррекция нарушения дыхания и сердечной деятельности. В зависимости от степени поражения ЦНС и тяжести состояния больных с тяжелыми формами отека, нарушения дыхания и сердечной деятельности могут быть первичными и вторичными. При их коррекции используются стандартные методики.
Этиологическое лечение основного заболевания. Рациональное лечение отека мозга заключается в устранении самой причины, которая этот отек вызвала. Такое лечение возможно лишь тогда, когда первопричина отека точно известна. Однако даже устранение причины отека не обязательно приводит к его ликвидации. В таких случаях терапевтические воздействия необходимо направить на сам отек мозга. Следует указать, что ни один метод лечения не устранит отек вокруг опухоли, абсцесса или гематомы, если не ликвидирован первичный патологический очаг.
Патогенетическая терапия отека направлена, в первую очередь, на устранение гипоксии как наиболее неблагоприятного фактора, способствующего развитию отека. Эта терапия направлена на нормализацию гемодинамики, ликвородинамики, метаболизма нейронов.
Иными словами, терапия нацелена на коррекцию основных патофизиологических механизмов (циркуляторных, васкуляторных, тканевых), участвующих в развитии отека мозга.
Коррекция гематоциркуляторных нарушений включает:
1. Лечебные мероприятия, направленные на нормализацию показателей системной гемодинамики. Для поддержания адекватной перфузии головного мозга необходимо сконцентрировать усилия на нормализацию системного артериального давления путем рационального назначения вазоактивных (дилататоров или констрикторов) препаратов быстрого действия (клофелин, дибазол или кофеин бензоат натрия и др.).
2. Назначение блокаторов кальциевых каналов. Эти препараты способствуют улучшению мозговой циркуляции, уменьшают накопление тканевых гормонов и тем самым обеспечивают устойчивость мозга к гипоксии. К ним относятся верапамил и его производные (финоптин, изоптин), нимодипин, лидофлазин, нифедипин (коринфар), фендилин (сензид), циннаризин (стугерон).
3. Усиление микроциркуляции мозга путем назначения препаратов, нормализующих тонус сосудов и реологические свойства крови. Здесь целесообразно использовать следующие вазоактивные препараты: кавинтон, ксантинола никотинат (компламин, теоникол, ксарин), эуфиллин, трентал (агапурин), дипиридамол (курантил), галидор, сермион (редергин), реополиглюкин, гепарин, индометацин (вольтарен, ортофен, аспирин).
При коррекции васкулярного (барьерного) фактора назначают следующие препараты:
• глюкокортикоиды (назначается либо преднизолон, либо дексаметазон);
• ингибиторы протеолитических ферментов. Они инактивируют тканевые гормоны воспаления при отеке головного мозга (гистамин, брадикинин, трипсин и др.). Для этой цели в/в вводится контрикал в дозе 1-10 тыс. ЕД/кг, гордокс — 12-15 тыс. ЕД/кг, аминокапроновая кислота — 200—300 мг/кг/24 ч. Курс лечения ингибиторами протеолитических ферментов, как правило, не превышает 5—7 дней;
• препараты, стабилизирующие клеточные мембраны и ангиопротекторы. Назначение последних способствует уменьшению проницаемости стенки сосудов мозга. К этой группе препаратов относятся дицинон, троксевазин, гливенол, венорутон, аскорутин;
• блокаторы кальциевых каналов (о назначении этих препаратов сказано выше);
• иммунокорригирующие препараты. В качестве иммуносупрессоров чаще всего используются стероидные гормоны (кортизон, гидрокортизон, преднизолон).
Иммуностимулирующая терапия включает применение тимозина, Т-активина, В-активина, тимогена, левамизола, пропермила, витаминов группы В.
Коррекция тканевого фактора включает:
• обеспечение адекватной оксигенации крови. Достигается восстановлением и поддержанием проходимости дыхательных путей, проведением постоянной ингаляции увлажненного кислорода, применением в некоторых случаях гипербарической оксигенации и ИВЛ;
• нормализацию метаболических процессов в нейронах головного мозга. Для этой цели используются ноотропы (ноотропил, пирацетам, ами-налон, церебролизин, энцефабол, пантогам, пиридитол и др.).
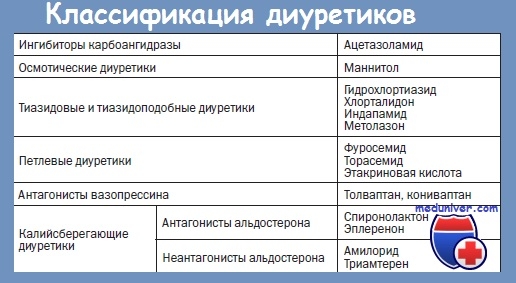
Коррекция нарушений водно-электролитного обмена и дегидратационная терапия. Важным патогенетическим направлением лечения отека мозга является назначение дегидратационной терапии:
• осмотические диуретики ( глицерин, маннитол, сорбитол и др.);
• салуретики (лазикс, фуросемид и др.);
• кортикостероиды (гидрокортизон, преднизолон). Следует указать, что действие стероидов на отек мозга развивается медленно — эффект обнаруживается не раньше, чем через 24 ч после первого введения препарата. Они более эффективны при локальных отеках мозга; кроме этого необходимо знать, что длительное применение стероидов, особенно в малых дозировках, может вызвать увеличение объема мозга и ВЧД;
• барбитураты (внутримышечно 10% раствор тиопентала натрия в дозе 10 мг/кг каждые 3 ч, суточная доза детям до 80 мг/кг).
Хирургическая коррекция отека мозга. Когда этиологический фактор отека мозга представлен экспансивным процессом (гематома, опухоль, абсцесс и т. д.), он может быть прерван только с помощью нейрохирургического вмешательства.
Экстренная медицина
 |
 |
 |
 |
.jpg) Лечение отека мозга должно быть комплексным и направленным на:
Лечение отека мозга должно быть комплексным и направленным на:
1) снижение внутричерепного давления и уменьшение гидрофильности мозговой ткани;
2) улучшение церебральной циркуляции;
3) нормализацию метаболизма и снижение энергетических потребностей мозга;
4) уменьшение проницаемости гемато-энцефалического барьера.
Изменения, происходящие в ткани мозга при отеке, сами по себе ухудшают условия оксигенации нервных клеток из-за увеличения размеров кроговского тканевого цилиндра и затруднения диффузии кислорода, что иногда находит отражение в увеличении капиллярно-ликворного градиента рО2 (Э. М. Николаенко, 1970). Эти данные подтверждают необходимость раннего проведения дегидратаци-онной терапии, направленной на уменьшение объема мозга, снижение внутричерепного давления и содержания воды в мозговой ткани. Наиболее эффективными дегидратационными средствами являются мочевина и маннитол.
Мочевину назначают внутривенно в виде 30% раствора в 10% растворе глюкозы из расчета 1 —1,5 г на 1 кг веса. В результате увеличения осмотического давления плазмы вода из отечной ткани мозга1 перемещается в сосудистый сектор, что сопровождается подъемом центрального венозного и артериального давления. Внутричерепное давление очень быстро снижается и уже через 30—60 мин после введения мочевины со скоростью 60 капель в 1 мин достигает самой низкой точки. К этому времени наблюдается выраженный диуретический эффект. Для своевременного выведения мочи и контроля диуреза катетеризируют мочевой пузырь.
Благоприятное действие мочевины на отечный мозг, по мнению М. Ш. Промыслова с сотрудниками (1966), связано не только с осмотическим фактором, но и с денатурацией и резким снижением гидрофильности белков мозга. Однако нужно иметь в виду, что дегидратационный эффект мочевины сохраняется не более 6ч, затем наблюдается регидратация мозга и к 12—18-му ч внутричерепное давление возвращается к исходному, а иногда и превышает его. Вторичное повышение внутричерепного давления — так называемый феномен отдачи — объясняется постепенным накоплением мочевины в ткани мозга, снижением ее концентрации в плазме, изменением направления осмотического градиента и регидратацией мозговой ткани, хотя некоторые авторы и отрицают такую возможность.
Другое популярное дегидратирующее средство — маннитол — имеет более крупную молекулу и обладает рядом преимуществ по сравнению с мочевиной. Он не вызывает азотемии, не противопоказан при поражениях почек и не приводит к столь выраженной «отдаче» внутричерепного давления, как мочевина. С целью дегидратации внутривенно вводят 1,5—2 г маниитола на 1 кг веса в 20% растворе. Важным является не только доза препарата, но и темп его введения. Всю дозу рекомендуется вводить в течение 30—60 мин. При этом наблюдается снижение давления спинномозговой жидкости на 50—90%, которое затем постепенно повышается, достигая исходного уровня через 4—8 ч.
При введении маннитола наблюдается еще более выраженное увеличение диуреза, чем при введении мочевины, сопровождающееся: значительным выведением электролитов. Однократная дегидратация, мочевиной или маннитолом обычно не приводит к нарушениям электролитного баланса. Однако при повторных введениях этих препаратов следует тщательно контролировать и корригировать водно-электролитные соотношения, объем циркулирующей крови, гематокрит и состояние гемодинамики. Маннитол можно применять в комбинации с мочевиной (В. Л. Данскер, 1968), с 30% раствором фруктозы (М1уагак1, Ма1зито1о, 1967) или с этакриновой кислотой (ШПкт-зоп е. а., 1971).
В последнее время все более широкое распространение при лечении-, отека “мозга получает глицерин. Его вводят в желудок через зонд вместе с фруктовыми соками из расчета 1,5—2 г на 1 кг веса.
Для внутривенного введения при остром отеке мозга используют 30% раствор глицерина (1—1,2 г/кг) на 20% растворе аскорбината натрия. Действие препарата начинает проявляться уже через 10— 15 мин, а через 1’/2—2 часа наблюдается максимальное снижение внутричерепного давления. К этому же времени значительно возрастает диурез.
Waterhaus, Сохоn (1970) и Меуеr (1971) показано, что глицерин не проникает через гемато-энцефалический барьер и поэтому не вызывает «отдачи» внутричерепного давления и это является его преимуществом перед другими осмотическими агентами. Однако нужно иметь в виду, что применение глицерина иногда может сопровождаться такими осложнениями, как рвота, эрозирование желудка и гематурия. Для профилактики этих осложнений глицерин назначают на голодный желудок с фруктовыми соками, дают больным обволакивающие и понижающие кислотность средства. Для этой цели может быть рекомендован альмагель. Использование в качестве растворителя аскорбината натрия предотвращает гематурию.
Концентрированный раствор альбумина или плазмы повышает онкотическое давление крови, что приводит к дегидратации ткани. Однако дегидратирующий эффект этих средств по отношению к мозгу ниже, чем у осмотических дегидратантов, поскольку они очень быстро притягивают в сосудистое русло воду из других тканей и гиперонкотичность утрачивается.
Мочегонные препараты также с успехом применяют для борьбы с отеком мозга и внутричерепной липертензией. С помощью фуросемида (лазикса 40—60 мг) или урегита (этакриноновая кислота 50—100 мг) при сохранной выделительной функции почек часто удается добиться значительного снижения внутричерепного давления. Механизм дегидратационного действия салуретиков связан с усиленным выделением воды из организма, сгущением крови и повышением ее осмотического и онкотического давления с последующим отвлечением воды из отечного мозга. Хорошее противоотечное действие оказывает сочетание концентрированных белковых препаратов с фуросемидом, а также урегита с маннитолом. В последнем случае этакриновую кислоту вводят за 20—30 мин до введения половинной дозы маннитола и получают в 11/2 раза более выраженный гипотензивный эффект. Длительное применение салуретиков сопровождается повышенным выведением электролитов и требует контроля и коррекции ионного состава крови с целью предотвращения гипокалиемии и гипохлоремического алкалоза.
Благоприятное действие осмо- и онкодегидратантов связано прежде .всего с уменьшением объема мозга, снижением внутричерепного давления, укорочением расстояний диффузии газов в мозговой ткани и увеличением эффективного перфузионного давления в церебральной сосудистой системе. В то же время за счет увеличения объема циркулирующей плазмы наблюдается снижение гематокрита и вязкости крови, повышение артериального давления и увеличение сердечного выброса, что приводит в свою очередь к увеличению мозгового кровотока и улучшению снабжения мозга кислородом. Под влиянием дегидратации мозговой кровоток увеличивается в среднем на 44%, а потребление кислорода возрастает на 25%.
Однако дегидратационный эффект, как правило, имеет временный характер и гипероемотичесиие средства при остром отеке мозга нужно назначать лишь для быстрого снижения внутричерепного давления и уменьшения компрессии мозга. Основные же усилия должны быть направлены на нормализацию метаболизма мозговой ткани. Для пополнения энергетических ресурсов мозга в условиях нарушенного окислительного гликолиза назначают 10—20% растворы глюкозы с инсулином, калием, АТФ и кокарбоксилазой. Инсулин не только способствует проникновению глюкозы в клетку, но и оказывает благоприятное воздействие на фермент, катализирующий реакцию перефосфорилирования глюкозы с АТФ. Имеются данные о том, что АТФ, введенный внутривенно, оказывает прямое воздействие на мозговую ткань и приводит к увеличению мозгового кровотока, потребления кислорода и глюкозы и к лучшению ЭЭГ. Показано также введение витаминов В1 В15, С.
С целью компенсации интрацеллюлярного ацидоза внутривенно назначают ТНАМ, который снижает концентрацию Н+-иона внутри клетки и тем самым способствует уменьшению отека мозга. При введении этого буфера необходимо тщательно контролировать состояние дыхания больных, поскольку в результате снижения локального рСО2 может развиться угнетение респираторного центра.
Искусственную вентиляцию легких у больных с отеком мозга следует начинать при появлении малейших признаков нарушения дыхания или сознания. Развитие гипоксической гипоксии в сочетании с гаперкапнией усугубляет набухание мозга и ведет к дальнейшему увеличению внутричерепной гипертензии. Искусственную вентиляцию легких проводят в режиме гипервентиляции при раСO2 25—30 мм рт. ст. Как правило, больные с нарастающим отеком мозга легко синхронизируются с респиратором; в противном случае внутривенно вводят раствор оксибутирата натрия (4—6 г), который сам по себе благоприятно действует на церебральный метаболизм и способствует уменьшению отека мозга.
Снижение напряжения углекислоты в крови и тканевой жидкости при отеке мозга целесообразно со многих точек зрения. Практически при любом поражении мозга наблюдаются нарушения церебрального кровообращения и метаболизма и выраженный ацидоз мозговой ткани, что приводит к расстройству функции клеточных мембран. Гипервенти-ляция уменьшает концентрацию Н+-ионов в мозге и способствует нормализации мембранных процессов. Уменьшение ацидоза мозговой ткани приводит также к улучшению циркуляции в пораженных участках мозга благодаря сужению сосудов в здоровых тканях, снижению внутричерепного давления и отвлечению крови в пораженнные зоны мозга из здоровых участков (феномен «обратного обкрадывания», синдром Робин Гуда. С помощью гипервентиляции удается снизить внутричерепное давление на 27—29% (Э. М. Николаевко, 1969. Искусственную вентиляцию легких проводят в объеме, превышающем расчетные величины в 11/2—2 раза. При этом нужно стремиться к тому, чтобы давление на вдохе не превышало 11—-12 см вод. ст., поскольку с повышением внутригрудного давления затрудняется венозный отток из мозговых сосудов и уменьшается положительное влияние гипокапнии на внутричерепную гипертензию. Выключение негативной фазы частично предотвращает повышение центрального венозного давления, однако чрезмерное разрежение на выдохе приводит к ухудшению выведения углекислого газа из-за эффекта «ловушки» и задержки воздуха в альвеолах.
Сосуды мозга постепенно адаптируются к гипокапнии и уже через сутки, несмотря на низкое рСО2, внутричерепной объем крови может достичь исходной величины. В этих условиях даже раCO2, близкое к 40 мм рт. ст., может оказаться «гиперкапническим» для мозговых сосудов, вызвать их дилятацию, резкое набухание мозга и повышение внутричерепного давления, в связи с чем не следует сразу (после гипервентиляции внезапно прерывать искусственную вентиляцию легких и переводить больных с отеком мозга на спонтанное дыхание.
Гипотермию при различных отеках мозга применяют во многих клиниках. При охлаждении тела до 30—32° наблюдается существенное уменьшение внутричерепной гипертензии вследствие сужения сосудов, уменьшения мозгового кровотока и сокращения размеров клеток мозга в результате понижения их метаболической активности. Потребность мозга в кислороде при гипотермии резко уменьшается, благодаря чему напряжение кислорода в ткани мозга всегда остается выше необходимого уровня, несмотря на уменьшенное кровоснабжение.
Наиболее показано применение гипотермии при лечении отека мозга у больных с тяжелой черепно-мозговой травмой, у нейрохирургических больных (Э. И. Кандель, Э. М. Николаенко, 1969); при гипоисических поражениях мозга (Бакай, Ли, 1969), а также при развитии отека мозга после операций на сердце (Т. М. Дарбинян, 1964). У больных же с внутримозговыми опухолями и при токсических отеках гипотермия не является методом выбора.
В клинической практике гипотермия (29—32°) может поддерживаться на протяжении до 2—3 нед. Такое охлаждение не маскирует неврологической симптоматики и позволяет наблюдать за ее динамикой. Важным преимуществом этого метода является отсутствие «отдачи» внутричерепного давления. Однако многие авторы отмечают, что при гипотермии могут развиваться расстройства электролитного баланса, метаболический ацидоз, нарушается свертываемость крови, а также возникает опасность фибрилляции желудочков сердца, хотя Rosomoff (1968) утверждает, что эта опасность становится реальной лишь при охлаждении ниже 28°. Серьезным недостатком гипотермии является сложность ее проведения. Многие осложнения и неудачи при лечении отека мозга с помощью гипотермии связаны именно с методическими погрешностями. Более простым и перспективным является метод кра-ниоцеребральной гипотермии с помощью специальных аппаратов.
Кортикостероидные гормоны приобретают все более широкое распространение при лечении отека мозга, хотя механизм их действия до сих пор остается не вполне понятным. Кортикостероиды стабилизирующе действуют на стенки капилляров, снижая их проницаемость, положительно влияют на церебральную микроциркуляцию, нормализуют функцию клеточных мембран, препятствуют накоплению воды и ионов Ка+ в ткани мозга, что обусловлено нормализацией работы «натриевой помпы» в результате восстановления НАДФ и окисления НАД • Н2. Хотя в обычных условиях стероиды, как известно, приводят к задержке воды и натрия в организме, при отеке они могут действовать парадоксально, приводя к увеличению диуреза и экскреции натрия, что связано с угнетением продукции антидиуретического гормона.
Особенно эффективны гормоны при отеках, сопровождающих опухоли, инсульты и травмы мозга. В зависимости от тяжести поражения и степени выраженности внутричерепной гипертензии внутривенно или внутримышечно назначают гидрокортизон до 1 г или преднизолон до-240 мг в сутки на протяжении нескольких дней или недель.
Синтетический препарат дексаметазон, который примерно в 7 раз активнее преднизолона, является, пожалуй, лучшим гормональным средством для лечения отека мозга, поскольку лишен минералокортикоидной активности и не приводит к задержке воды и солей. Лечение начинают с внутривенного введения 10 мг этого препарата и затем назначают по 4 мг дексаметазона через 4—6 ч внутримышечно. Терапевтический эффект начинает проявляться через 12—18 ч, а максимальный эффект кортикостероидов наблюдается лишь через несколько дней. Отличных результатов при лечении отека мозга добились Ferrari и Ragonese, назначая внутривенно 25 ед. АКТГ в 250 мл 5% раствора глюкозы с окситоцином в возрастающей дозе на 1—8 ед. дважды в сутки на протяжении недели.
При длительном применении стероидов их дозировку необходимо снижать постепенно в течение 5—7 дней, поскольку внезапная отмена может сопровождаться резким увеличением отека мозга. Следует иметь в виду, что кортикостероидная терапия может маскировать симптоматику внутричерепной геморрагии.
В комплекс медикаментозных средств при лечении отека мозга включают также центральные холинолитики — амизил или метамизил по 2—5 мг в сутки (П. П. Денисенко, 1962), которые обладают умеренным антигистаминным и антисеротониновым свойством, способствуют поляризации глиальных клеток и влияют на гаалуроновую кислоту (В. М. Самвелян, 1968). Холинолитики подавляют афферентную импульсацию из патологических очагов мозга и снижают возбудимость некоторых подкорковых центров, что имеет важное значение для профилактики и лечения отека мозга. По тем же соображениям назначают ганглиоблокаторы (пентамин, арфонад, гигроний) (Э. И. Кандель, 1957; Э. И. Злотник, 1965) и новокаин внутривенно в виде глюкозо-новокаиновых смесей, или, как рекомендуют А. Д. Гагулашвили и В. Р. Мансая (1961), для лечения травматических отеков мозга-внутрикаротидно по 7—10 мл 0,25% раствора.
Эуфиллин вводят внутривенно по 10 мл 2,4% раствора 2—3 раза в сутки с целью улучшения мозгового и почечного кровообращения. Назначают также аспирин и бутадиен, которые являются ингибиторами-брадикинина и способствуют дезагрегации форменных элементов крови, улучшая тем самым церебральную микроциркуляцию (А. 3. Маневич и др.). Применение фенотиазиновых препаратов-(аминазин, пипольфен) патогенетически оправдано благодаря их адренолитическому действию, поскольку повышенный выброс катехоламинов играет важную роль в развитии отека мозга.
При острых быстро нарастающих отеках мозга, сопровождающихся симптомами вклинения ствола (при опухолях и черепно-мозговых травмах), нейрохирургам иногда приходится прибегать к широкой декомпрессивной трепанации со вскрытием твердой мозговой оболочки и рассечением мозжечкового намета. Применяют введение физиологического раствора в спинномозговой канал с целью реклинации ствола мозга, ущемленного в большом затылочном отверстии, и вентрикулярный дренаж.
В настоящее время представляется перспективным лечение церебрального отека с помощью гипербарической оксигенации, имеющей к тому теоретические и экспериментальные предпосылки.
Руководство по клинической реаниматологии, под ред. проф. Т.М. Дарбиняна, 1974
Отек мозга: общие сведения, причины, симптомы и лечение
Отек мозга – угрожающее жизни состояние, возникающее при травмах головы, гидроцефалии и инсультах. Смещение мозговых тканей приводит к повреждению клеток (цитотоксическому фактору) или нарушению проницаемости мембран головного мозга (вазогенному фактору). Распространенными причинами являются инфаркты мозга, черепно-мозговая травма – бытовая или спортивная, более редкими – опухоли и менингиты.
Общие сведения
Отек головного мозга развивается на фоне ишемического или геморрагического инсульта, черепно-мозговых травм, повышает вероятность летального исхода. Состояния развивается из-за недостаточности мембранных транспортеров и гематоэнцефалического барьера. При развитии отека сочетаются цитотоксические, ионные и вазогенные механизмы. Для лечения используют декомпрессионную краниэктомию и осмотерапию. Но эти методы не влияют на патологический молекулярный каскад, приводящий к отеку.
Причины отека головного мозга
Отек головного мозга возникает на фоне различных неврологических и других патологических состояний:
- Энцефалиты из-за укуса клещей, в качестве осложнений после гриппа.
- Инфекционные факторы нейроцистицеркоз (паразитарное поражение головного мозга), церебральная малярия или менингиты.
- Инсульты ишемические, геморрагические и эмболические.
- Гидроцефалия, как последствие менингита или травм.
- Ишемическая энцефалопатия при родовых травмах, высоком артериальном давлении, атеросклерозе.
- Венозный тромбоз внутричерепных синусов.
- Опухоли головного мозга.
К заболеваниям, провоцирующим отек мозга, относится диабетический кетоацидоз, печеночная недостаточность, нарушения электролитного баланса. Симптомы отека мозга могут проявиться не сразу.
Церебральный отек у детей с гидроцефалией связан с увеличенным внутричерепным давлением.

Кто в группе риска
К группе высокого риска относятся люди с тяжелой формой диабетического кетоацидоза, а также дети, у которых ацидоз произошел впервые. Факторами, повышающими вероятность отека, являются: обезвоживание, воспалительный процесс и сгущение крови.
В результате снижается приток крови к головному мозгу, возникает каскад реакций ишемии и отека. Повышается внутричерепное давление, снижается артериальное давление и частота сердечных сокращений. Грыжа мозга может сжимать жизненно важные структуры в стволе мозга. Пациенты с гиперактивным течением кетоацидоза подвержены большему риску. Высокие уровни аммиака выше 200 мкмоль/л в крови могут быть индикатором риска развития внутричерепной гипертензии.
При гепатической энцефалопатии к церебральному отеку приводит снижение перфузионного давления сосудах мозга, отек клеток астроцитов из-за скопления аммиака и повышения выработки глутамина. На фоне отека растет внутричерепное давление, развивается ишемический ушиб и грыжа мозга.
Зачастую отек мозга развивается у детей, перенесших гипоксию, и имеющих гидроцефалию. Церебральная эдема может осложнять течение инсультов и черепно-мозговых травм.
Патогенез
Набухание головного мозга — это ступенчатый процесс, при котором острое повреждение приводит к образованию цитотоксического, ионного или вазогенного отека. Что такое отек? Это комбинация патогенетических механизмов. Цитотоксический отек характеризуется истощением внутриклеточного аденозинтрифосфата (АТФ), который нарушает активный транспорт осмолитов через клеточные мембраны. В клетках происходит накопление ионов натрия и воды.
На поверхности клеточных мембран нарушается давление и соотношение ионов, что приводит движению жидкости во внеклеточное пространство паренхимы мозга из сосудов. Этот механизм еще называется ионным. При ушибах мозга повышается активность ионного канала Sur1-Trpm4 в эндотелиальных клетках, что приводит к скоплению жидкости.
Отдельная форма цитотоксического отека – вазогенный. Патология развивается из-за повышенной проницаемости гематоэнцефалического барьера головного мозга после ушиба, выброса воспалительных веществ при инфекции и увеличения свободных радикалов. В результате происходит выделение жидкости вне клетки вместе с протеинами плазмы крови.

По мере развития ушиба мозга данные механизмы сменяют и дополняют друг друга, приводя к набуханию. Считается, что отеку предшествует повышение внутричерепного давления из-за фиксированного объема закрытой полости черепа. Одновременно снижается капиллярная перфузия – давление крови в сосудах мозга. Ткани недополучают питательные вещества и кислород, развивается гипоксемия.
Классификация
Отек головного мозга возникает из-за увеличенного содержания мозговой жидкости. В патогенезе развития эдемы условно разделяют три формы: цитотоксическую, вазогенную и интерстициальную или их комбинацию.
Вазогенный отёк
Вазогенный отек – наиболее распространенная форма, вызванная нарушением гематоэнцефалического барьера. Белки плазмы проникают за пределы сосудов, из-за чего осмотическое давление нагнетает жидкость в интерстициальное пространство головного мозга. Например, эндотелиальный фактор роста, глутамат и лейкотриены локально повышают проницаемость клеток вокруг опухоли. Именно это, наряду со слабостью сосудистых стенок, приводит к попаданию жидкости с белками в паренхиму белого вещества. Отеки возле опухолей в 65% приводят к когнитивным нарушениям у пациентов из-за смещения мозговых структур.
Вазогенный отек провоцируется нарушением проницаемости сосудов и изменением перфузионного давления на фоне следующих заболеваний и состояний:
- абсцесс мозга;
- инсульт;
- гиперкапния;
- энцефалопатия на фоне гипертонии;
- гепатическая энцефалопатия;
- метаболические нарушения;
- диабетический кетоацидоз;
- отравление свинцом;
- горная болезнь.
Патогенные микроорганизмы при менингитах нарушают проницаемость гематоэнцефалического барьера для белков и ионов натрия. Это приводит к накоплению жидкости в межклеточном пространстве, а также набуханию клеток из-за пассивной гипоксии. Повышенное внутричерепное давление нарушает связи между нейронами.
Цитотоксический отёк
Клеточный или цитотоксический отек возникает внутри клеток без повреждения гематоэнцефалического барьера. Развивается патология после инсульта или черепно-мозговой травмы с повреждением глиальной ткани, нейронов и эндотелиальных клеток. В клетках нарушается гемостатический механизм, и натрий накапливается в них, нарушается выход ионов за пределы оболочки. Анионы стараются восстановить нейтральность на поверхности мембраны, что приводит к отеку внутри клетки.
Цитотоксический связан с изменением ионного баланса на поверхности клеточных мембран в результате нескольких причин:
- гипоксическая ишемическая травма головного мозга (при утоплении, остановке сердца);
- травма головного мозга;
- метаболические нарушения обмена органических кислот;
- гепатическая энцефалопатия;
- синдром Рея (острая печеночная недостаточность);
- инфекции (энцефалиты и менингиты);
- диабетический кетоацидоз;
- интоксикации (аспирином, этилен гликолем, метанолом);
- гипонатриемия или избыточное потребление воды без электролитов.
Интерстициальный отёк
Одна из основных причин интерстициального отека – обструктивная гидроцефалия. Интерстициальный отек развивается из-за подтекания спинномозговой жидкости из желудочков мозга в интерстициальное пространство мозга. Пациенты с гидроцефалией или менингитом предрасположены к данной патологии. Увеличенное давление в желудочках приводит к вытеснению содержимого желудочков, что приводит к отеку белого вещества.
Симптомы отека головного мозга
Отек мозга в зависимости от степени изменений может быть бессимптомным или симптоматическим. Тяжесть проявлений зависит от возраста человека. У детей отек компенсируется наличием родничков, и потому симптоматика отличается.
Отек головного мозга имеет различные проявления:
- изменения сознания, в том числе кома;
- головные боли и мигрени;
- эпилепсия;
- интоксикация;
- кишечная непроходимость (заворот кишки, инвагинация)
- неврит зрительного нерва;
- гипертрофический пилоростеноз
- макроцефалия.
Общемозговые симптомы связаны с повышением внутричерепного давления:
- При медленном повышении пациентов беспокоят утренние головные боли, рвота без тошноты, что характерно для опухолей головного мозга. Возникают преходящие головокружения. Медленно меняется поведение: пациенты становятся раздражительными, капризными.
- При быстром повышении боль приступообразная, распирающая, сильная. Рвота не дает облегчения. У пациентов повышаются сухожильные рефлексы, замедляется сердцебиение и двигательные реакции. Меняются движения глаз, наступает сонливость, нарушается речь и мышление.
При декомпенсации повышенного внутричерепного давления развивается кома, а при смещении структур мозга – нарушение дыхания, сердечных сокращений.
Диагностика отека мозга
Ранняя диагностика отека мозга снижает смертность и улучшает функциональные возможности пациентов после ишемического инсульта. При установлении патологии проводят декомпрессионную трепанацию. Нарастание отека мозга можно определить по симптомам увеличения внутричерепного давления: учащения эпизодов потери сознания, тошноты и рвоты, головной боли, нарушению зрения, гемипарезу. Среди перечисленных признаков именно бессознательное состояние, связанное с поражением ретикулярной активирующей системы и таламо-гипоталамической-кортикальной оси, считается самым важным клиническим параметром. Степень поражения сознания измеряется по шкале комы Глазго.
При геморрагическом инсульте существуют другие критерии оценки риска отека мозга. Вероятность увеличения гематомы возрастает при изначальном значительном ее размере, использовании антикоагулянтов, раннем появлении симптомов. Риск развития отека увеличивается при гипергликемии, повышенном артериальном давлении, большом размере гематомы и увеличении перфузионного церебрального давления.


Лечение отека головного мозга
Задача интенсивной терапии – поддерживать дыхание и нормальные показатели гемодинамики. Голова пациента находится на возвышении на высоте 30 градусов для оттока венозной крови. Начинают раннее энтеральное питание.
Применяются следующие методы терапии:
- искусственная вентиляция легких при симптомах дислокации мозга;
- гипервентиляция при условии мониторинга уровня насыщения кислородом крови;
- введение гиперосмолярных растворов;
- барбитуратовая кома;
- трепанация черепа;
- гипотермия (снижение температуры тела).
Протоколы терапии отека зависят от его причины. При вазоспазме важно увеличение объема плазмы крови, а при гиперемии – диуретики и гипервентиляция.
Консервативные методы
Осмотерапия – это базовая медикаментозной терапия при отеках головного мозга. Ее редко используют для профилактики из-за ограниченной эффективности из-за раннего применения. Гиперосмолярные средства создают внутрисосудистый осмотический градиент, который облегчает выведение воды. Чаще всего применяют маннитол и гипертонический физиологический раствор. Последний помогает расширить внутрисосудистый объем, увеличить сократимость сердца и внутричерепное давление.
Осмотический диурез с маннитом может вызвать внутрисосудистую дегидратацию и гипотензию, и после него необходимо обеспечить адекватную замену жидкости изотоническими растворами. Длительное повторное применение гипертонического физиологического раствора приведет к развитию гиперхлоремического метаболического ацидоза. Потому средства используют в качестве альтернативы для лечения симптоматического отека мозга.
Хирургические методы
Хирургическое вмешательство позволяет избежать летальных исходов при обширных полушарных инсультах. Особенно у пациентов в возрасте до 60 лет, если процедура проводится на протяжении 48 часов после появления симптомов. Декомпрессионная хирургия проводится на ранней стадии развития отека, удаляется костный диаметром не менее 12 см. После декомпрессии врачи следят за развитием субдурального кровоизлияния, наружной гидроцефалии, предотвращают инфицирование раны и расхождения кровеносных сосудов.
Хирургия применяется для удаления образования, которое вызывает отек мозга – внутримозговой гематомы, абсцесса или опухоли. Удалению подлежат гематомы в коре размерами более 3 см, а также в области мозжечка – более 2 см.
Особенности терапии цитотоксического отёка
Лечение цитотоксического отека проводят с помощью маннитола или другого осмодиуретика. Маннитол используют в дозировке 0,5-1 г на килограмм массы тела внутривенно. Эффективность осмотических средств сохраняется первые 48-72 часов. При цитотоксическом отеке стараются не снижать артериальное давление, если сохранены механизмы ауторегуляции. Внутривенно вводят растворы для увеличения объема циркулирующей крови, проводят вазопрессорную терапию. Подход применяют при сохранении гематоэнцефалического барьера. Барбитуровый наркоз уменьшает отечность. Тиопентал натрия вводят для снижения внутричерепного давления ниже 20 мм рт. ст.
Особенности терапии вазогенного отёка
Вазогенный отек требует использования ангиопротекторных препаратов. Эсцинулизинат восстанавливает тонус сосудистых стенок, усиливает реабсорбцию и снижает интерстициальный отек. При вазогенных отеках используют глюкокортикоиды для снижения проницаемости гематоэнцефалического барьера. Обычно дексаметазон вводят одновременно с антибиотиками при менингитах. Маннитол при вазогенном отеке наоборот усиливает поступление жидкости в ткани. Для защиты паренхимы мозга применяют антиоксиданты и средства для улучшения метаболизма (актовегин, кортексин).
Прогноз
Отек мозга после инсульта у взрослых развивается под действием ряда факторов. К эпидемиологическим относится история гипертонии или ишемической болезни сердца в анамнезе. Важный клинический критерий — оценка по неврологической шкале NIHSS при инсульте выше 20 в доминирующем полушарии или более 15 в не доминирующем. Развитие тошноты и рвоты первые сутки после инсульта. Систолическое артериальное давление выше 180 мм рт.ст. первые 12 часов после приступа. Снижение реакций на раздражители.
Определить риск отека мозга можно по МРТ:
- окклюзия крупных артерий;
- поражение большого количества сосудов;
- аномалии Виллизиева круга.
- очаг инфаркта более 82 мл спустя 6 часов после появления симптомов;
- очаг более 145 ил спустя 14 часов после первых признаков.
При черепно-мозговых травмах еще до госпитализации важно приступить к нейропротекторной терапии, введению кортикостероиодов и диуретиков, что улучшает прогноз у молодых пациентов.
Какие варианты развития возможны
Зависимо от распространения отека выделяют три синдрома его развития:
- Общемозговой – связан с ростом внутричерепной гипертензии. Головная боль, рвота, нарушения зрения, снижение пульса на фоне роста САД и нарушение мышления.
- Синдром рострокаудального нарастания – распространение отека на кору, подкорковые структуры и ствол мозга. При повреждении коры появляются судороги, подкорковых областей – гиперкинезы, патологические рефлексы. Нарушение сознания означает повреждение гипоталамуса. Стволовые повреждения проявляются угнетением дыхания и сердечно-сосудистой деятельности.
- Синдром дислокации проявляется выпадением функции глазодвигательных нервов, ригидностью мышц затылка, нарушением глотания.
При вклинении ствола мозга в большое затылочное отверстие многие изменения необратимы.
Последствия отека мозга
Осложнения отека мозга связаны с присоединением инфекции в виде пневмонии, пиелонефритов и менингитов. Развиваются трофические нарушения, тромбозы.
Чем опасен отек? При компрессии ствола возможно развитие паралича. Даже после оптимального лечения и восстановления остаются спайки в мозговых оболочках, что приводит к депрессии, головным болями. Последствия отека головного мозга включают психические расстройства, снижение когнитивных функций.
Причины и последствия отека головного мозга
Из статьи вы узнаете о причинах и механизме развития отека головного мозга, симптомах, диагностике, лечении и прогнозе патологии.

Общие сведения
Набухание головного мозга было описано еще в 1865 году Н.И. Пироговым. На сегодняшний день стало понятно, что отек головного мозга не является самостоятельной нозологической единицей, а представляет собой вторично развивающийся патологический процесс, возникающий как осложнение целого ряда заболеваний.
Следует отметить, что отек любых других тканей организма — достаточно часто встречающееся явление, совсем не относящееся к ургентным состояниям. В случае головного мозга, отек является жизнеугрожающим состоянием, поскольку, находясь в замкнутом пространстве черепа, церебральные ткани не имеют возможности увеличиваться в объеме и оказываются сдавленными. Вследствие полиэтиологичности отека мозга, в своей практике с ним сталкиваются как специалисты в области неврологии и нейрохирургии, так и травматологи, неонатологи, онкологи, токсикологи.
Этиология заболевания
Наиболее часто отек головного мозга развивается при травмировании или органическом поражении его тканей. К таким состояниям относятся: тяжелая ЧМТ (ушиб головного мозга, перелом основания черепа, внутримозговая гематома, субдуральная гематома, диффузное аксональное повреждение, операции на головном мозге), обширный ишемический инсульт, геморрагический инсульт, субарахноидальное кровоизлияние и кровоизлияние в желудочки, первичные опухоли головного мозга (медуллобластома, гемангиобластома, астроцитома, глиома и др.) и его метастатическое поражение. Отек церебральных тканей возможен как осложнение инфекционных заболеваний (энцефалита, менингита) и гнойных процессов головного мозга (субдуральной эмпиемы).
Наряду с внутричерепными факторами к отеку мозга может привести анасарка, возникшая вследствие сердечной недостаточности, аллергические реакции (отек Квинке, анафилактический шок), острые инфекции (токсоплазмоз, скарлатина, свиной грипп, корь, паротит), эндогенные интоксикации (при тяжелом течении сахарного диабета, ОПН, печеночной недостаточности), отравления различными ядами и некоторыми медикаментами.
В отдельных случаях отек головного мозга наблюдается при алкоголизме, что связано с резко повышенной сосудистой проницаемостью. У новорожденных отек мозга бывает обусловлен тяжелым токсикозом беременной, внутричерепной родовой травмой, обвитием пуповиной, затяжными родами. Среди любителей высокогорного спорта встречается т. н. «горный» отек мозга, являющийся результатом слишком резкого набора высоты без необходимой акклиматизации.
Патогенез
Основным звеном в развитии церебрального отека выступают микроциркуляторные нарушения. Первоначально они, как правило, возникают в области очага поражения мозговой ткани (участка ишемии, воспаления, травмы, кровоизлияния, опухоли). Развивается локальный перифокальный отек головного мозга. В случаях тяжелого поражения головного мозга, не проведения своевременного лечения или отсутствия должного эффекта последнего, возникает расстройство сосудистой регуляции, ведущее к тотальному расширению церебральных сосудов и подъему внутрисосудистого гидростатического давления. В результате жидкая часть крови пропотевает через стенки сосудов и пропитывает церебральную ткань. Развивается генерализованный отек головного мозга и его набухание.
В описанном выше процессе ключевыми компонентами являются сосудистый, циркуляторный и тканевой. Сосудистым компонентом выступает повышенная проницаемость стенок мозговых сосудов, циркуляторным — артериальная гипертензия и расширение сосудов, которые приводят к многократному повышению давления в церебральных капиллярах. Тканевой фактор заключается в склонности тканей головного мозга при недостаточности кровоснабжения накапливать жидкость.
В ограниченном пространстве черепной коробки 80-85% объема приходится на церебральные ткани, от 5 до 15% — на цереброспинальную жидкость (ликвор), около 6% занимает кровь. У взрослого нормальное внутричерепное давление в горизонтальном положении варьирует в пределах 3-15 мм рт. ст. Во время чихания или кашля оно ненадолго поднимается до 50 мм рт. ст., что не вызывает расстройств функционирования ЦНС. Отек головного мозга сопровождается быстро нарастающим повышением внутричерепного давления за счет увеличения объема церебральных тканей. Происходит сдавление сосудов, что усугубляет микроциркуляторные нарушения и ишемию мозговых клеток. Вследствие метаболических нарушений, в первую очередь гипоксии, возникает массовая гибель нейронов.
Кроме того, резкая внутричерепная гипертензия может приводить к дислокации нижележащих церебральных структур и ущемлению ствола мозга в большом затылочном отверстии. Нарушение функции находящихся в стволе дыхательного, сердечно-сосудистого и терморегуляторного центров является причиной многих летальных исходов.
Классификация патологии
Отек головного мозга возникает из-за увеличенного содержания мозговой жидкости. В патогенезе развития эдемы условно разделяют три формы: цитотоксическую, вазогенную и интерстициальную или их комбинацию.
Вазогенный отек
Вазогенный отек – наиболее распространенная форма, вызванная нарушением гематоэнцефалического барьера. Белки плазмы проникают за пределы сосудов, из-за чего осмотическое давление нагнетает жидкость в интерстициальное пространство головного мозга. Например, эндотелиальный фактор роста, глутамат и лейкотриены локально повышают проницаемость клеток вокруг опухоли. Именно это, наряду со слабостью сосудистых стенок, приводит к попаданию жидкости с белками в паренхиму белого вещества. Отеки возле опухолей в 65% приводят к когнитивным нарушениям у пациентов из-за смещения мозговых структур.
Вазогенный отек провоцируется нарушением проницаемости сосудов и изменением перфузионного давления на фоне следующих заболеваний и состояний:
- абсцесс мозга;
- инсульт;
- гиперкапния;
- энцефалопатия на фоне гипертонии;
- гепатическая энцефалопатия;
- метаболические нарушения;
- диабетический кетоацидоз;
- отравление свинцом;
- горная болезнь.
Патогенные микроорганизмы при менингитах нарушают проницаемость гематоэнцефалического барьера для белков и ионов натрия. Это приводит к накоплению жидкости в межклеточном пространстве, а также набуханию клеток из-за пассивной гипоксии. Повышенное внутричерепное давление нарушает связи между нейронами.
Цитотоксический отек
Клеточный или цитотоксический отек возникает внутри клеток без повреждения гематоэнцефалического барьера. Развивается патология после инсульта или черепно-мозговой травмы с повреждением глиальной ткани, нейронов и эндотелиальных клеток. В клетках нарушается гемостатический механизм, и натрий накапливается в них, нарушается выход ионов за пределы оболочки. Анионы стараются восстановить нейтральность на поверхности мембраны, что приводит к отеку внутри клетки.
Цитотоксический связан с изменением ионного баланса на поверхности клеточных мембран в результате нескольких причин:
- гипоксическая ишемическая травма головного мозга (при утоплении, остановке сердца);
- травма головного мозга;
- метаболические нарушения обмена органических кислот;
- гепатическая энцефалопатия;
- синдром Рея (острая печеночная недостаточность);
- инфекции (энцефалиты и менингиты);
- диабетический кетоацидоз;
- интоксикации (аспирином, этилен гликолем, метанолом);
- гипонатриемия или избыточное потребление воды без электролитов.
Интерстициальный отек
Одна из основных причин интерстициального отека – обструктивная гидроцефалия. Интерстициальный отек развивается из-за подтекания спинномозговой жидкости из желудочков мозга в интерстициальное пространство мозга. Пациенты с гидроцефалией или менингитом предрасположены к данной патологии. Увеличенное давление в желудочках приводит к вытеснению содержимого желудочков, что приводит к отеку белого вещества.
Симптомы и клинические проявления
Клинически признаки отечности можно разделить на общемозговые и очаговые. Симптомы отека мозга, их чередование и совмещение друг с другом зависят от первопричины данного заболевания. В связи с этим выделяют постепенные и молниеносные формы отечности. В первом случае, есть время на предупреждение прогрессирования отека, а во втором – остается только борьба за жизнь и замедление на некоторое время прогрессирования патологии.
У взрослых
- Помутнение сознания. Проявляется при всех типах отека ГМ и бывает разной выраженности: от ступора до глубокой комы. С дальнейшим нарастанием отека глубина обморочного состояния увеличивается.
- При походке нарушается равновесие.
- Головная боль. Бывает по причине хронических и нарастающих острых заболеваний мозга.
- Снижение зрения.
- Падение давления, сонливость, слабость.
- Тошнота, сопровождающаяся рвотой.
- Судороги, вплоть до потери сознания (больной прикусывает язык).
- Нарушения дыхания.
У детей
Основные симптомы отека мозга у детей дополняются вялостью, слабостью, головной болью, могут появляться или усиливаться парез и паралич, отекает сосок зрительного нерва.
При прогрессировании патологии возникают судороги, нарушаются функции сердечно-сосудистой системы, нарастает симптоматика. Клиническая картина такова:
- некупируемая гипертермия;
- головная боль;
- возбужденное состояние;
- «мозговой» крик;
- выбухание родничка;
- ригидность затылочных мышц;
- кома;
- сопор;
- острая почечная недостаточность;
- симптомы затылочного и височно-теменного вклинения мозга: косоглазие, анизокория, нарушение витальных функций (синдром дислокации структур мозга);
- окуломоторный криз с фиксацией взгляда и расширением зрачков, тахикардия, повышенный мышечный тонус, гипертермия, нестабильность давления (синдром компрессии среднего мозга);
- мидриаз, рвота, анизокория, утрата сознания (синдром сдавления ствола);
- брадипноэ, брадикардия, дисфагия, рвота, парестезии (нарушение чувствительности) в плечевом поясе, ригидность затылочных мышц, остановка дыхания (синдром ущемления мозжечка).
Диагностика

Предположить наличие у пациента ОГМ можно на основании следующих признаков:
- нарастающее угнетение сознания;
- прогрессирующее ухудшение общего состояния;
- наличие менингеальных симптомов.
Для подтверждения диагноза показано выполнение компьютерной или магниторезонансной томографии головного мозга.
Диагностическая люмбальная пункция проводится в исключительных случаях и с большой осторожностью, так как может спровоцировать дислокацию мозговых структур и сдавление ствола.
Для выявления возможной причины ОГМ проводят:
- оценку неврологического статуса;
- анализ данных КТ и МРТ;
- клиническое и биохимическое исследование крови;
- сбор анамнестических данных (при возможности).
ОГМ является опасным для жизни человека состоянием. Поэтому первичная диагностика должна проводиться в максимально короткие сроки и начинаться с первых минут поступления пациента в стационар. В тяжелых случаях диагностические мероприятия осуществляют одновременно с оказанием первой медицинской помощи.
Особенности лечения
Задача интенсивной терапии – поддерживать дыхание и нормальные показатели гемодинамики. Голова пациента находится на возвышении на высоте 30 градусов для оттока венозной крови. Начинают раннее энтеральное питание.
Применяются следующие методы терапии:
- искусственная вентиляция легких при симптомах дислокации мозга;
- гипервентиляция при условии мониторинга уровня насыщения кислородом крови;
- введение гиперосмолярных растворов;
- барбитуратовая кома;
- трепанация черепа;
- гипотермия (снижение температуры тела).
Протоколы терапии отека зависят от его причины. При вазоспазме важно увеличение объема плазмы крови, а при гиперемии – диуретики и гипервентиляция.
Консервативные методы
Осмотерапия – это базовая медикаментозной терапия при отеках головного мозга. Ее редко используют для профилактики из-за ограниченной эффективности из-за раннего применения. Гиперосмолярные средства создают внутрисосудистый осмотический градиент, который облегчает выведение воды. Чаще всего применяют маннитол и гипертонический физиологический раствор. Последний помогает расширить внутрисосудистый объем, увеличить сократимость сердца и внутричерепное давление.
Осмотический диурез с маннитом может вызвать внутрисосудистую дегидратацию и гипотензию, и после него необходимо обеспечить адекватную замену жидкости изотоническими растворами. Длительное повторное применение гипертонического физиологического раствора приведет к развитию гиперхлоремического метаболического ацидоза. Потому средства используют в качестве альтернативы для лечения симптоматического отека мозга.
Адекватная оксигенация и улучшение метаболизма мозга достигаются путем:
- Инстилляций увлажненного кислорода или искусственной вентиляции легких;
- Местной гипотермии путем обкладывания вокруг головы емкостей, заполненных льдом;
- Введения препаратов, улучшающих обменные процессы в пораженных клетках мозга (актовегин, мескидол, цераксон, кортексин);
- Глюкокортикоидные гормоны. Их действие заключается в мембраностабилизиции пораженных клеток и укреплении ослабленной сосудистой стенки микроциркуляторного русла.
Хирургические методы
Хирургическое вмешательство позволяет избежать летальных исходов при обширных полушарных инсультах. Особенно у пациентов в возрасте до 60 лет, если процедура проводится на протяжении 48 часов после появления симптомов. Декомпрессионная хирургия проводится на ранней стадии развития отека, удаляется костный диаметром не менее 12 см. После декомпрессии врачи следят за развитием субдурального кровоизлияния, наружной гидроцефалии, предотвращают инфицирование раны и расхождения кровеносных сосудов.
Хирургия применяется для удаления образования, которое вызывает отек мозга – внутримозговой гематомы, абсцесса или опухоли. Удалению подлежат гематомы в коре размерами более 3 см, а также в области мозжечка – более 2 см.
Устранение причины и сопутствующих симптомов
Отек мозга в большинстве случаев сопровождается различными мозговыми и внемозговыми проявлениями, которые стали его причиной или следствием.
Поэтому обязательно мониторятся и корригируются:
- Состояние сердечной деятельности;
- Признаки интоксикации и ее последствия;
- Повышение температуры тела, которая усугубляет отек мозга.
- Повлиять на причину отека мозга можно только после ее точного установления.
Потенциально полезными для устранения причин могут оказаться:
- Антибактериальная терапия препаратами, обладающими высокой проникающей способностью в отношении гематоэнцефалического барьера (цефуроксим, цефепим);
- Выведение токсических соединений из организма;
- Удаление операбельных опухолей внутричерепной локализации, но только после стабилизации состояния больного;
- Ликвородренирующие операции, заключающиеся в создании обходных путей ликвора, что снизит внутричерепное давление и уменьшит опасность отека мозга.
Решение проблем, связанных с отеком мозга – нелегкая задача. Заниматься ее решением должны исключительно профессионалы.
Осложнения
При значительном повышении внутричерепного давления может наблюдаться дислокация (смещение) структур мозга и ущемление его ствола в большом затылочном отверстии. Это приводит к тяжелым поражениям дыхательного, сосудодвигательного и терморегуляторного центра, что может стать причиной летального исхода на фоне нарастающей острой сердечной и дыхательной недостаточности, гипертермии.
Прогноз
В начальной стадии развития ОГМ представляет собой обратимое состояние, но по мере прогрессирования патологического процесса происходит гибель нейронов и разрушение миелиновых волокон, что приводит к необратимым повреждениям мозговых структур. При раннем начале лечения ОГМ токсического генеза у молодых и исходно здоровых пациентов можно ожидать полного восстановления мозговых функций.
Во всех остальных случаях будут отмечаться остаточные явления различной степени выраженности:
- стойкие головные боли;
- рассеянность;
- забывчивость;
- депрессия;
- нарушения сна;
- повышение внутричерепного давления;
- расстройства двигательных и когнитивных функций;
- расстройства психики.
Профилактика
Меры первичной профилактики отека головного мозга направлены на предотвращение причин, лежащих в основе его развития. Они могут включать в себя:
- профилактику производственного, дорожно-транспортного и бытового травматизма;
- своевременное выявление и активное лечение артериальной гипертензии и атеросклероза, являющихся основными причинами инсульта;
- своевременную терапию инфекционно-воспалительных заболеваний (энцефалитов, менингитов).
Если у пациента имеется патология, на фоне которой возможно развитие церебрального отека, то ему обязательно проводят профилактическое лечение, направленное на предотвращение набухания вещества головного мозга. Оно может включать в себя:
- поддержание нормального онкотического давления плазмы (внутривенное введение гипертонических растворов, альбумина, свежезамороженной плазмы);
- назначение при высоком внутричерепном давлении мочегонных средств;
- искусственная гипотермия – позволяет уменьшить энергетические потребности клеток головного мозга и тем самым предотвращает их массовую гибель;
- применение препаратов, улучшающих тонус церебральных сосудов и обменные процессы в мозговых тканях.
Однако в подавляющем большинстве случаев у выживших пациентов наблюдаются остаточные явления перенесенного отека головного мозга. Они могут значительно варьировать от малозаметных окружающим симптомов (головной боли, повышенного внутричерепного давления, рассеянности, забывчивости, нарушений сна, депрессии) до выраженных инвалидизирующих расстройств когнитивных и двигательных функций, психической сферы.
Что вызывает отёк мозга
Отёк мозга возникает в результате скопления ликвора в мозговых тканях, что повышает внутричерепное давление. Запускается механизм отмирания клеток мозга. Заболевание характеризуется серьёзными последствиями и требует неотложной медицинской помощи.

Отёк головного мозга – болезнь, при которой затрудняется отток цереброспинальной жидкости. Это приводит к повышению внутричерепного давления и затруднению подачи крови к мозговым тканям. Развивается некроз. При отсутствии своевременного лечения патология вызывает смерть.
Характеристика понятия
У здорового человека ликвор циркулирует в межцеребральном мозговом пространстве, питая ткани и защищая их от повреждения. В результате воздействия отрицательных факторов повышается объём спинальной жидкости, что вызывает серьёзные нарушения и осложнения. Проявления отёка головного мозга быстро нарастают, состояние больного резко ухудшается.
Любопытный факт! Впервые болезнь описал Н. Пирогов в 1865 году.
Отёчность нарушает проницаемость сосудистых стенок, блокирует выход крови в окружающие тканевые структуры. В результате развития патологических процессов молекулы воды проникают через мембрану в нервные сплетения. Там клетки взаимодействуют с белками, увеличиваясь в объёмах.
Отёк мозга не может выступать самостоятельным заболеванием, патология развивается вторично в качестве осложнения иных болезней. Заболевание угрожает жизни человека, поскольку церебральные структуры сдавливаются в результате увеличения их объёма. Прогрессирование процесса приводит к защемлению мозговых структур, которые отвечают за терморегуляцию, дыхание, сердечную деятельность.
Классификация
Отёк головного мозга подробно охарактеризован международной классификацией заболеваний. Этот факт облегчает диагностирование патологии, что позволяет начать лечение своевременно.
Обратите внимание! Нужно различать отёки, которые развиваются вследствие различных заболеваний, с перифокальной отёчностью, когда набухание мозга происходит после полученных травм.
Отёки дифференцируют, исходя из этиологии нарушения:
- Вазогенный, вызывается увеличенной сосудистой проницаемостью. Центральная и кровеносная системы разделены анатомическим барьером – гематоэнцефалическим. Отёк развивается при прохождении экссудата через барьер. Это приводит к повышению объёмов белого вещества. Развивается в результате внутреннего кровоизлияния, повреждения центральной нервной системы, возникновения новообразований.
- Гидростатический. Образуется при повышении давления вентикулярного типа. В основном диагностируется у младенцев. У взрослых выявляется изредка, после хирургических вмешательств, черепно-мозговых травм, когда фиксируется вклинивание костных частей в мозговое вещество.
- Цитотоксический. Формируется вследствие интоксикации клеток головного мозга в результате облучения, отравления, а также после инсультов. Нарушается тканевый метаболизм. Остановить гибель клеток можно в первые часы прогрессирования патологии, затем процесс становится необратимым.
- Осмотический. Мозговая жидкость включает мельчайшие растворённые частицы, концентрация которых на килограмм ликвора носит название осмолярности. При нарушениях в соотношении частиц и плазмы мозга развивается отёчность. В результате повышения количества частиц в экссудате ткани пытаются снизить их объём, поглощая влагу из плазмы. Подобный дисбаланс возникает вследствие водного воздействия на мозг, гипергликемии, энцефалопатии.
Отдельно выделяют отёк мозга у новорождённых, который появляется вследствие внутриутробной гипоксии, неправильного развития эмбриона, полученных травм в процессе родоразрешения.
В зависимости от параметров мозгового поражения выделяют локальный, диффузный и генерализованный отёк. Дислокация локального вида фиксируется в очаге поражения, диффузного – в одном полушарии, генерализванного – в обоих полушариях.
Исходя из причины появления, отёк бывает токсическим, травматическим, гипертензивным, ишемическим, послеоперационным, опухолевым, воспалительным.
Отёчность может затрагивать мозговые сосуды, вещество либо ствол мозга. Последнее состояние наиболее опасно, поскольку оно сопровождается нарушением дыхания и кровоснабжения.
Что вызывает мозговую отёчность
Мозговые ткани отекают вследствие воздействия причин инфекционного либо травматического характера.
Черепно-мозговые травмы
Травмы, раны с вклинением черепных частей, сотрясения блокируют эвакуацию жидкости, вызывая прогресс некротических процессов. Травматическое набухание осложняется повреждением мягких тканей. Это приводит к проблемам с передвижением, судорожным припадкам, парализации ног.
К этой группе относится отёчность, возникающая вследствие операций, трепанации черепа. После хирургического вмешательства в область головы зачастую образуется рубец, который затрудняет циркуляцию жидкости.
Болезни инфекционного характера
Отёк головного мозга возникает в результате острого воспалительного явления. Патологический симптом развивается на фоне менингита, энцефалита, токсоплазмоза. При образовании гнойных включений состояние человека резко ухудшается.
Опухолевые новообразования
Раковые опухоли давят на мягкие ткани, вызывая раздражение и отёчность структур. После устранения образования отёк быстро спадает. Пациенту требуется длительное реабилитационное лечение.
Кровоизлияние
Разрыв артериальных стенок происходит в результате наличия атеросклеротических бляшек, аневризмы, травмы головы. Подобное состояние имеет высокий процент летальности.
Инсульт
Ишемическая болезнь сердца возникает в результате образования тромба в артерии. Это провоцирует острую кислородную недостаточность и некроз тканей. Отмирание клеточных структур вызывает отёчность.
Отек мозга – экстренные меры и правильное лечение

В клетках и промежуточном пространстве главного регулирующего органа центральной нервной системы может накапливаться жидкость. Это приводит к отеку или набуханию мозга, которое провоцирует увеличение его объема и повышение внутричерепного давления. Данное состояние считается крайне опасной патологией, требующей немедленного лечения.
Отек мозга – виды
Классификация рассматриваемой болезни основывается на механизмах ее возникновения и последующего течения. Существует отек головного мозга таких типов:
- вазогенный;
- цитотоксический;
- интерстициальный;
- осмотический (фильтрационный).
Дополнительно отек мозга может дифференцироваться в зависимости от причин его образования:
- опухолевый;
- травматический;
- воспалительный;
- токсический;
- послеоперационный;
- гипертензивный;
- ишемический и другие варианты.
Вазогенный отек головного мозга
Между кровеносной и центральной нервной системой существует физиологическое препятствие – гемато-энцефалический барьер (ГЭБ). С его помощью регулируется содержание воды в межклеточном пространстве. При повышении проницаемости ГЭБ возникает вазогенный отек мозга. Он встречается на фоне следующих нарушений:
- холодовая травма;
- опухоли;
- газовая и микроэмболия сосудов;
- эклампсия;
- окклюзия сонных артерий.
Цитотоксический отек головного мозга
Клетки, подверженные отравляющему воздействию (внешнему или внутреннему), начинают функционировать неправильно. Меняется их метаболизм и проницаемость мембран. Ткань накапливает жидкость и развивается цитотоксический отек или набухание. Указанная форма патологии часто диагностируется после инсультов и сильных интоксикаций, но она обратима в течение первых 6-8 часов.
Интерстициальный отек головного мозга
В главном органе центральной нервной системы постоянно циркулирует ликвор или цереброспинальная жидкость, преимущественно в желудочках. Когда давление в них резко и сильно повышается, возникает интерстициальный отек мозга. Описываемое состояние провоцирует пропитывание тканей лишним ликвором. В результате клетки увеличиваются в объеме и набухают.
Осмотический отек головного мозга
Любая жидкость содержит растворенные в ней частицы. Их количество в 1 кг влаги называется осмолярностью. В норме данный показатель для плазмы и руководящего органа нервной системы почти идентичен. Если наблюдается гиперосмолярность (слишком высокая) «серого вещества», устанавливается диагноз «отек мозга». Из-за увеличения объема частиц в ликворе ткани стремятся снизить их концентрацию, и поглощают жидкость из плазмы. Такой отек мозга регистрируется при энцефалопатиях метаболического типа. Его часто вызывает гипергликемия, почечная и печеночная недостаточность.

Отек головного мозга – причины
Самые распространенные факторы, провоцирующие рассматриваемое осложнение:
- острые нарушения кровообращения (инсульты);
- хирургические вмешательства;
- сильные интоксикации, включая алкогольное отравление;
- анафилактические реакции на фоне аллергии.
Есть и менее часто встречающиеся причины, которые объясняют, от чего бывает отек мозга:
- раковые опухоли и метастазы;
- переломы костей черепного свода и основания;
- декомпенсированная почечная, печеночная, сердечная недостаточность;
- менингит;
- ушиб мозга;
- посттравматические внутричерепные гематомы;
- диффузное аксональное повреждение;
- менингоэнцефалит;
- токсоплазмоз;
- субдуральная эмпиема.
Отек мозга после инсульта
Нарушение кровообращения в главном органе центральной нервной системы начинается с закупорки сосуда тромбом. Постепенно к тканям поступает все меньше кислорода, из-за чего развивается их кислородное голодание. Клетки отмирают и активно впитывают любую влагу, возникает ишемический отек мозга. В некоторых случаях биологическая жидкость, скапливающаяся перед тромбом, может разорвать стенки сосуда. Это явление утяжеляет отек мозга при инсульте, потому что ткани после кровоизлияния поглощают еще больше влаги. Данный вариант набухания клеток считается самым опасным.
Отек мозга после операции
Патология практически всегда сопровождает хирургические вмешательства в области черепа. В редких случаях и на фоне других процедур возникает отек мозга – операция, выполненная с применением эпидуральной анестезии, или избыточным введением гипотонических и солевых растворов внутривенно. Иногда набухание клеток происходит вследствие осложнений хирургического вмешательства:
- крупные кровопотери;
- некорректная интубация трахеи для искусственной вентиляции легких;
- продолжительное и выраженное снижение артериального давления;
- неправильно рассчитанная анестезия.
Алкогольный отек мозга
Чрезмерное количество этилового спирта в организме приводит к тяжелому отравлению. У алкоголиков очень часто диагностируется отек мозга – причины состоят в длительной интоксикации клеток, из-за чего необратимо меняется их метаболизм и функционирование. Поврежденные ткани поглощают влагу, провоцируя набухание и расширение. Такой отек мозга характерен и при отравлениях другими веществами:
- ядовитые химические соединения;
- наркотики;
- токсичные газы;
- медикаменты.
Отек мозга при аллергии
Неадекватная реакция иммунной системы на раздражители у некоторых людей сопровождается анафилактическим шоком. В таких случаях фактор, провоцирующий отек мозга – аллергия. На фоне гиперчувствительности резко уменьшается интенсивность кровотока во всем организме, значительно снижается артериальное давление и развивается коллапс. Из-за отсутствия достаточного кровоснабжения жизненно важных структур клетки «серого вещества» впитывают жидкость и набухают.
Отек головного мозга – симптомы
Клиническая картина описываемой патологии всегда идентична и не зависит ни от ее причин, ни от механизмов развития. Есть 3 группы признаков, характеризующих отек мозга – симптомы делятся на следующие типы:
- Синдром внутричерепной гипертензии. Вследствие набухания тканей значительно увеличивается их объем. Избыток жидкости в черепной коробке приводит к сильному возрастанию давления. Это провоцирует тошноту, распирающую и невыносимую головную боль, неукротимую рвоту. Если отек мозга продолжается долго, наблюдается ухудшение сознания.
- Очаговые клинические проявления. Набухание тканей в определенных отделах управляющего органа центральной нервной системы вызывает нарушение их специфических функций. В результате отмечаются параличи, зрительные, речевые расстройства, ухудшение координации движений. Иногда больной совершенно не способен на осуществление высшей нервной деятельности и пребывает в бессознательном состоянии.
- Стволовые признаки. Отек-набухание мозга может привести к смещению некоторых структур органа, сдавливанию увеличенными объемами тканей близлежащих нервных окончаний и кровеносных сосудов. На фоне таких явлений наблюдается нарушение сердечной и дыхательной деятельности, ухудшение кровообращения, угнетение реакции зрачков и другие угрожающие жизни патологии.
Отек головного мозга – лечение
Слабо выраженная степень заболевания, например, после сотрясения или нетяжелого ушиба, не нуждается в специальной терапии. Такие варианты набухания тканей проходят самостоятельно в течение 2-4 суток. Госпитализация необходима, если прогрессирует сильный отек мозга – лечение сложных и опасных видов патологии осуществляется только в отделении реанимации.

Основной целью терапии является нормализация церебрального перфузионного давления (ЦПД). Оно отвечает за кровоснабжение, поступление кислорода и питательных веществ к нейронам. ЦПД представляет собой разность между средним артериальным и суммой внутричерепного и центрального венозного давления. Другие задачи лечения:
- устранение судорог и двигательного перевозбуждения;
- поддержание нормальной температуры тела;
- восстановление функций легких и сердца;
- нормализация деятельности поврежденных отделов мозга;
- удаление причин, препятствующих оттоку венозной крови из черепной полости;
- купирование и предупреждение болевого синдрома;
- выведение избытка жидкости из тканей.
Отек мозга – неотложная помощь
Больных с указанным диагнозом тяжелой степени следует немедленно госпитализировать.
Первая доврачебная помощь:
- Обнаружив признаки отека мозга, сразу вызвать бригаду медиков.
- Положить пострадавшего на горизонтальную поверхность.
- Обеспечить приток свежего воздуха.
- При наличии рвоты повернуть голову человека на бок.
- Расстегнуть или снять сдавливающую одежду.
- В случае возникновения судорог аккуратно придерживать голову и конечности больного, предотвращая нанесение ушибов и травм.
Отек мозга – препараты
Для выведения избытка жидкости из клеток и церебральных тканей применяется дегидратационная терапия. Если обнаружен выраженный отек мозга у взрослых, сначала назначается внутривенное введение осмотических диуретиков с помощью капельницы – Маннитола, Альбумина и аналогов. После купирования острого состояния больного переводят на петлевые мочегонные:
Когда внутричерепное давление слишком высокое и устранить отек мозга перечисленными препаратами не удается, рекомендуется вентрикулостомия. Это хирургическое вмешательство, которое позволяет извлечь лишнюю жидкость из тканей. Процедура представляет собой введение канюли (полой толстой иглы) в один из желудочков мозга с целью создания дренажа. Такая манипуляция обеспечивает мгновенную нормализацию давления и отток лишней жидкости.
На фоне набухания мозга часто возникает гипоксия. Для купирования кислородного голодания и восстановления дыхательной деятельности проводится оксигенотерапия. Самый простой вариант – применение специальной маски с подачей концентрированного газа. В современных клиниках осуществляется оксигенобаротерапия – помещение пациента в особую воздушную среду с повышенным давлением кислорода. В тяжелых случаях экстренно выполняется искусственная вентиляция легких.

Чтобы улучшить церебральный метаболизм и нормализовать функции клеток мозга используется местное охлаждение головы и введение лекарственных растворов, активизирующих обменные процессы:
- Кортексин;
- Армадин;
- Мексидол;
- Цитиколин;
- Антифронт;
- Элфунат;
- Мексиприм;
- Венокор;
- Никомекс;
- Мексимидол;
- Динар;
- Замексен;
- Нейротропин-Мексибел.
Отек-набухание мозга сопровождается проницаемостью клеточных мембран и ослаблением сосудистых стенок. Справиться с этими нарушениями помогают глюкокортикостероидные гормоны:
Для стабилизации артериального давления назначаются:
Многим пациентам требуется купирование психомоторного возбуждения. С данной целью применяются:
Восстановление работы центральной нервной системы обеспечивают ангиопротекторы, гемостатики, антигиноксанты, ингибиторы протеолитических ферментов и другие группы медикаментов, которые включают следующие средства:
Иногда необходимо использование антибиотиков, преимущественно цефалоспоринов с широким спектром действия:
- Цефепим;
- Цефуроксим;
- Цефазолин;
- Цефадроксил;
- Цефтриаксон и аналоги.
Отек головного мозга – последствия
В редких случаях докторам удается полностью ликвидировать набухание тканей. Чаще осложняется отек мозга – последствия:
- психические расстройства;
- когнитивные нарушения;
- параличи и парезы;
- инвалидность (зависит от пораженных отделов головного мозга);
- рассеянность;
- расстройства сна;
- депрессия;
- проблемы с памятью;
- хронические головные боли;
- повышенное внутричерепное и артериальное давление;
- ухудшение двигательной активности.
Отек мозга – прогноз для жизни
Рассмотренная патология прогрессирует очень быстро, купировать ее без осложнений можно только при токсическом набухании тканей у молодых и здоровых людей. В остальных случаях возникают последствия после отека мозга разной степени тяжести. Прогноз зависит от обширности повреждения органа, затронутых отделов и выраженности сопутствующих нарушений. В большинстве ситуаций набухание мозга провоцирует необратимые осложнения, иногда отек приводит к гибели человека.