Гранулоцитопения: причины и лечение
Гранулоцитопения относится к категории заболеваний кровеносной системы. Это состояние, сопровождающееся снижением числа гранулоцитов в крови. При этом общее количество лейкоцитов обычно также снижается, но в некоторых случаях остается нормальным.
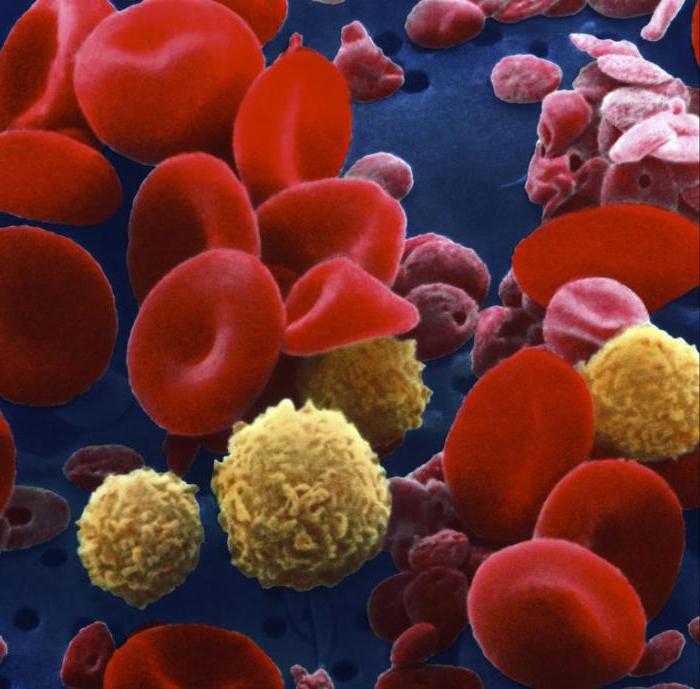
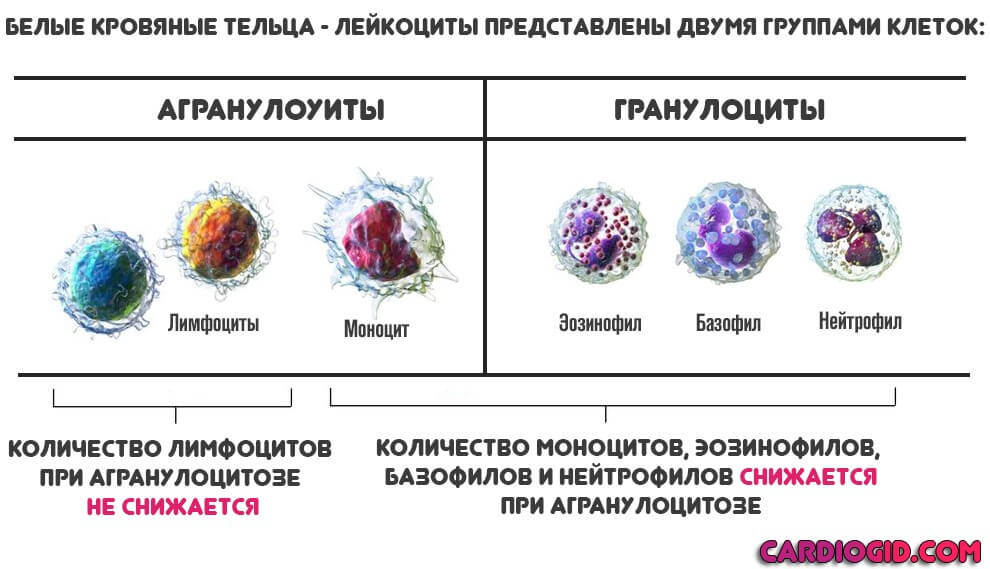
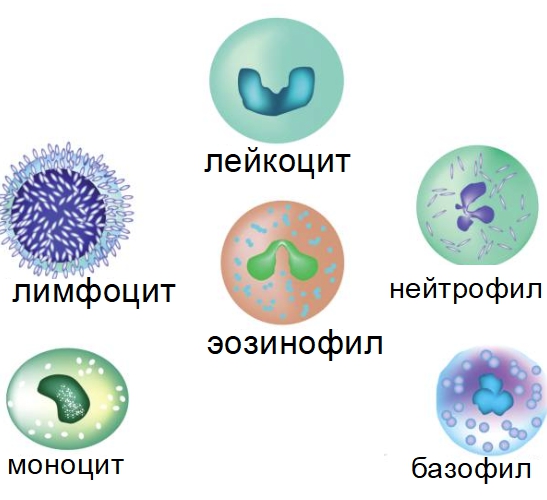
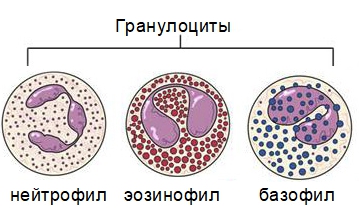
Гранулоциты являются одним из типов белых кровяных клеток, называемых лейкоцитами. Собственно, лейкоциты подразделяются на зернистые, т.е. гранулоциты, и агранулоциты (незернистые).
В свою очередь, к группе гранулоцитов относят нейтрофилы, базофилы и эозинофилы. Такое разделение обусловлено реакцией зернистых клеток на обработку различными красящими веществами. Так, на эозинофилы действует кислая краска, т.е. эозин, на базофилы – щелочная, т.е. гематоксилин, на нейтрофилы – оба вида красок, т.е. в данном случае последняя группа клеток проявляет нейтральные свойства по отношению к красящим компонентам: отсюда и такое название.
Функции гранулоцитов
Свойства гранулоцитов обусловлены наличием микрогранул, содержащих ферменты, которые выполняют важную для организма роль: уничтожают патогенные микроорганизмы.
Таким образом, гранулоциты являются необходимой частью системы иммунитета человека, так как реагируют на опасные антигены, которые попадают извне в организм.
При заметном недостатке гранулоцитов в крови в первую очередь снижается иммунитет, ведь клетки, выполняющие роль фагоцитов («пожирателей» чужеродных клеток), не успевают делать свою работу и своевременно уничтожать опасные микроорганизмы. В этом случае организм становится уязвим перед любыми микробами, в изобилии имеющимися на различных предметах, в воздухе и даже в самом теле человека.
Разновидности гранулоцитопении
В зависимости от типа гранулоцитов, содержание которых в крови патологически уменьшается, гранулоцитопению разделяют на такие разновидности:
- нейтропения – при дефиците нейтрофилов;
- базопения – при недостатке базофилов;
- эозинопения – при дефиците эозинофилов.
Достоверно определить разновидность недуга можно лишь после выполнения детального анализа крови.
Так, диагноз нейтропении (одной из разновидностей гранулоцитопении) может быть поставлен, если содержание нейтрофилов в образце крови значительно отклоняется от нормы, которая составляет 1500/1 мкл.
Исходя из этого, определяют стадии заболевания:
- легкая – если указанный показатель составляет более 1000 нейтрофилов, содержащихся в 1 мкл;
- среднетяжелая – от 500 до 1000 в 1 мкл;
- тяжелая – ниже 500 нейтрофилов в расчете на 1 мкл.
Заболевание может протекать в острой (развивающейся за несколько дней) или хронической форме. Опасной считается острая и одновременно тяжелая форма недуга.
Причины гранулоцитопении
Спровоцировать развитие гранулоцитопении может воздействие некоторых факторов:
- бактериальные инфекции, особенно поражение легких, кожи и гортани;
- генетическая предрасположенность;
- синдром Рихтера, являющийся врожденным заболеванием, проявляющимся болезнями крови, в том числе гранулоцитопенией;
- заболевания костного мозга, в том числе апластическая анемия, лейкоз, миелофиброз и др.;
- отравление некоторыми растениями, например, подофиллом щитовидным. Это небольшое растение содержит вещества, применяемые в медицине для выведения бородавок и папиллом. Плоды подофилла съедобны лишь в небольшом количестве. При злоупотреблении возможно отравление, сопровождающееся изменениями в составе крови;
- патологические нарушения в ретикулоцитах. Вследствие этого нарушения макрофаги начинают уничтожать гранулоциты и другие клетки крови;
- сокращение синтеза гранулоцитов в структурах костного мозга. Подобное воздействие на процесс образования клеток оказывают прием наркотиков и лучевая терапия;
- гиперспленизм – чрезмерное разрушение кровяных клеток в сезеленке;
- применение отдельных лекарств, в частности – некоторых антиаритмических средств, антибиотиков, антиметаболитов. Следовательно, длительный прием подобных препаратов опасен патологическими изменениями в составе кровяных клеток;
- значительный дефицит некоторых витаминов, особенно В12 и фолиевой кислоты;
- воздействие отдельных веществ, применяемых при химиотерапии при онкологических недугах;
- отрицательное влияние радиационной терапии.
Иногда причину гранулоцитопении установить достаточно сложно, особенно при первичном осмотре пациента, поэтому врач назначает для этой цели необходимые обследования.
Симптомы гранулоцитопении
Так как гранулоцитопения относится к числу довольно редких заболеваний, сам пациент далеко не всегда может поставить себе такой диагноз. Кроме того, по наличию отдельных симптомов практически невозможно заподозрить именно это заболевание крови.
Клиническая картина при развитии гранулоцитопении обычно обусловлена симптомами основной болезни. Так как при появлении этого недуга в крови резко падает количество гранулоцитов, выполняющих роль фагоцитов («защитников» организма от инфекций), то любое бактериальное заболевание может протекать в самой тяжелой форме.
Даже простые респираторные недуги в этом случае протекают довольно мучительно, не говоря уж о гриппе или бронхите. Больной гранулоцитопенией пациент также рискует заболеть туляремией, милиарным туберкулезом, брюшным тифом и прочими опасными заразными недугами.
Следовательно, если инфекции буквально «липнут» к человеку, протекают в тяжелой форме, значит, можно заподозрить наличие гранулоцитопении или иного заболевания крови.
Подтвердить подозрение или быстро развеять опасения поможет сдача несложных анализов.
Диагностика
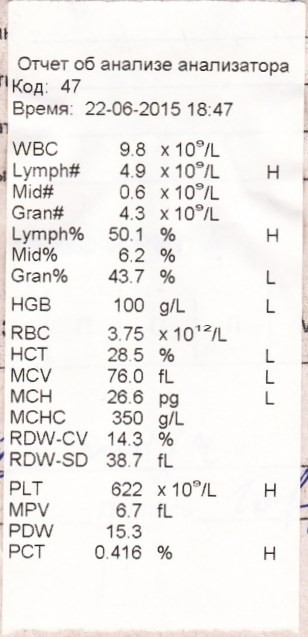
С целью диагностирования гранулоцитопении обычно назначают анализы крови, в том числе общий и биохимический. При необходимости выполняют более подробные анализы образца крови, а также исследование костного мозга.
У пациента высока вероятность гранулоцитопении, если:
- в крови число лейкоцитов заметно снижено;
- имеются только единичные гранулоциты в образцах крови;
- выявлена выраженная нейтропения;
- при пункции костного мозга обнаружены крайне незрелые образцы клеток, являющихся предшественницами гранулоцитопоэза (процесса образования гранулоцитов).
Диагностируется гранулоцитопения путем тщательного подсчета клеток крови и обработки результатов других анализов.
Лечение гранулоцитопении
При подтверждении диагноза гранулоцитопении пациенту назначают такие лечебные мероприятия:
- назначение препаратов, стимулирующих образование гранулоцитов в тканях костного мозга;
- отказ от приема лекарств, которые могли послужить причиной развития недуга;
- избегание воздействия радиации, некоторых токсичных веществ;
- отказ от употребления копченых, маринованных продуктов, а также пищи с плесенью;
- борьба с последствиями инфекций, которые могли развиться после снижения числа гранулоцитов в крови или обусловить подобное состояние;
- прием антибиотиков для ликвидации бактериальной инфекции, а также для профилактики;
- при необходимости назначение противогрибковых лекарств;
- в тяжелых случаях – обеспечение больному стерильных условий в специальном помещении, которое регулярно обрабатывают ультрафиолетом с целью дезинфекции;
- применение кортикостероидов или иммуноглобулинов, если именно гормональные или аутоиммунные нарушения привели к появлению гранулоцитопении;
- назначение витаминов при наличии признаков нехватки этих веществ;
- лечение основной болезни, которая могла стать причиной гранулоцитопении, путем приема противовоспалительных или иных средств.
Как не допустить развития гранулоцитопении?
Профилактика гранулоцитопении состоит в следующем:
- максимально возможное уменьшение контакта с реальными или потенциальными носителями инфекции;
- уменьшение или исключение воздействия на организм целого ряда токсичных веществ: бензина, клея, лаков, нефти, красок, различных растворителей, пестицидов;
- снижение потребления тех видов продуктов, которые обрабатывались консервантами, пестицидами, а также исключение из рациона испорченной или не вполне качественной пищи;
- недопущение потребления лекарств, особенно антибиотиков, обезболивающих препаратов, сульфаниламидов, без назначения специалиста;
- своевременное и максимально качественное лечение имеющихся недугов, особенно инфекционно-воспалительного характера;
- контроль за воздействием радиации на организм. Недопущение превышения максимально возможной дозировки облучения.
Обратите внимание! Воздействие провоцирующих факторов на организм каждого человека всегда индивидуально. Некоторые люди остаются здоровыми, даже получив значительную дозу опасного ионизирующего облучения. Другие же могут серьезно заболеть после мимолетного контакта с токсичными веществами.
В полной мере избежать влияния всех факторов практически невозможно, но если поддерживать состояние своего здоровья на должном уровне, полноценно питаться и сохранять приемлемый уровень физической активности, можно минимизировать риск заболеваний крови, в том числе гранулоцитопении.
Поддержание нормального состава крови особенно важно, ведь даже незначительное снижение числа гранулоцитов, в частности – нейтрофилов, заметно снижает сопротивляемость организма по отношению ко всевозможным инфекциям. При этом даже относительно безобидные бактерии, постоянно обитающие на поверхности кожи или слизистых различных органов, могут вызвать тяжелые недуги. Именно поэтому профилактика является важнейшим звеном в борьбе со столь серьезным заболеванием.
Совинская Елена, медицинский обозреватель
18,793 просмотров всего, 5 просмотров сегодня
Моноцитоз
Моноцитоз – это патологическое состояние, при котором наблюдается увеличение содержания моноцитов больше 1000 в 1 мкл крови. Причинами служат инфекционные, воспалительные, а также онкогематологические заболевания. У детей наиболее частой причиной выступает инфекционный мононуклеоз. Специфических симптомов нет. Клиническая картина определяется основной патологией. Уровень моноцитов исследуется в капиллярной или венозной крови при подсчете лейкоцитарной формулы. Для возврата моноцитов к референсным показателям (от 1 до 10%) проводится лечение болезни, послужившей фоном для возникновения моноцитоза.
Классификация
Четких цифровых разделений моноцитоза нет. Условно различают умеренный и выраженный моноцитоз. По патогенетическому механизму выделяют:
- Реактивный моноцитоз. Причиной данной разновидности являются воспалительные и инфекционные патологии.
- Неопластический (злокачественный) моноцитоз. Встречается у больных миелопролиферативными и лимфопролиферативными заболеваниями (у детей при лимфогранулематозе и остром монобластном лейкозе).
У детей с момента рождения наблюдается небольшое повышение моноцитов, оно достигает максимума к концу 1 недели жизни (до 15%), далее медленно снижается и к 12 месяцу становится как у взрослых.
Причины
Реконвалесценция
Несмотря на большое многообразие патологических причин, чаще всего моноцитоз свидетельствует о выздоровлении после острого инфекционного заболевания. Как правило, в основном это наблюдается у детей. Повышение уровня моноцитов после инфекции означает, что произошла полная элиминация инфекционного агента. Моноцитоз обычно незначительный, может сохраняться до 2-х недель, затем уровень моноцитов возвращается к нормальным показателям.
Вирусные инфекции
Моноциты являются первой линией противоинфекционной защиты. Мигрируя в ткани, они превращаются в мононуклеарные фагоциты (макрофаги). При проникновении микроорганизма (бактерии, вируса) макрофаги его поглощают (фагоцитируют), а также презентируют на своей поверхности чужеродные антигены патогена для распознавания их Т- и B-лимфоцитами. Кроме того, макрофаги выделяют широкий спектр различных медиаторов и цитокинов, вызывая хемотаксис нейтрофилов к очагу инфекционного воспаления. Нередко вирусные инфекции, кроме моноцитоза, становятся еще и причиной увеличения лимфоцитов (лимфомоноцитоз).
- Острые вирусные инфекции. Из всех заболеваний, самой распространенной причиной моноцитоза среди взрослых являются грипп, ОРВИ (парагрипп, аденовирусная, риновирусная инфекции). Обычно моноцитоз незначительный, он возникает резко наряду с симптоматикой, затем уменьшается до нормы примерно через 1-2 недели после стихания воспалительного процесса.
- Инфекционный мононуклеоз. Еще одной вирусной причиной моноцитоза, особенно часто встречающейся у детей, признан инфекционный мононуклеоз, вызванный вирусом Эпштейн-Барра. Ввиду длительного персистирования вируса в организме, моноцитоз может сохраняться несколько месяцев и даже лет. Также в острый период мононуклеоза в крови появляется большое количество лимфоцитов, приобретающих моноцитарные морфологические свойства (атипичных мононуклеаров) – увеличивается размер клетки и клеточного ядра, цитоплазма становится базофильной.
Бактериальные инфекции
Моноцитоз характерен для хронических бактериальных инфекций, сопровождающихся эпителиоидноклеточной пролиферацией с образованием гранулем. В первую очередь к ним относятся туберкулез, бруцеллез, сифилис. Также моноцитоз встречается при подостром бактериальном эндокардите, риккетсиозах. Патогенез повышения содержания моноцитов в крови при этих заболеваниях несколько отличается от такового от вирусных инфекций.
Причиной считается неэффективный фагоцитоз. Макрофаги, поглотив бактерии, не способны уничтожить их внутри себя, так как многие из этих бактерий устойчивы к разрушительному действию лизосомальных ферментов макрофагов. Вследствие этого они выступают убежищем для бактерий, защищая их от других иммунных клеток, и, позволяя им размножаться, участвуют в формировании гранулемы. Выделяя цитокины, макрофаги стимулируют образование новых моноцитов в костном мозге, обеспечивая бактерии новыми «убежищами».
Таким образом поддерживается хроническое течение болезни. Повышение концентрации моноцитов умеренное, из-за хронического течения патологии может сохраняться месяцами, годами, опускается до нормальных цифр только после этиотропного лечения. Единственной острой бактериальной инфекцией, вызывающей моноцитоз у детей, признана скарлатина.
Системные гранулематозные процессы
Хронические неинфекционные системные воспалительные заболевания также сопровождаются моноцитозом, механизм развития которого заключается в следующем. По неизвестным причинам запускается клеточно-опосредованная иммунная реакция. Макрофаги (тканевые моноциты), наряду с лимфоцитами и тучными клетками начинают скапливаться в различных органах, постепенно образуя гигантоклеточные гранулемы. Секретируя интерлейкины, цитокины и другие медиаторы, макрофаги поддерживают хроническое воспаление.
У взрослых причиной становятся саркоидоз, гистиоцитоз из клеток Лангерганса, гранулематоз Вегенера. Из системных гранулематозных патологий у детей чаще встречаются воспалительные заболевания кишечника (неспецифический язвенный колит, болезнь Крона). Моноцитоз умеренной степени, но несколько выше, чем при бактериальных и вирусных инфекциях, снижается под влиянием патогенетического лечения.
Диффузные болезни соединительной ткани
Причины моноцитоза при коллагенозах точно неизвестны. Существует теория, что под влиянием аутоантител к различным компонентам соединительной ткани и цитокинов стимулируется костномозговое созревание моноцитов. Также изучена роль моноцитов в индукции и поддержании хронического воспаления. Причиной моноцитоза у взрослых выступают системная красная волчанка, системная склеродермия, у детей в основном наблюдается дермато- и полимиозит. Степень моноцитоза коррелирует с активностью заболевания, во время ремиссии находится в пределах референсных значений.
Злокачественные болезни крови
Довольно частой причиной моноцитоза являются онкогематологические заболевания. Механизм увеличения количества моноцитов заключается в опухолевой трансформации стволовых клеток костного мозга. Моноцитоз очень высокий, клетки могут составлять более 50% от общего числа лейкоцитов. Моноцитоз сохраняется длительное время, снижается только после лечения химиотерапевтическими препаратами или трансплантации костного мозга.
Для взрослых более характерен хронический миелолейкоз. У детей причинами моноцитоза чаще выступают лимфогранулематоз (лимфома Ходжкина), острый монобластный (моноцитарный) лейкоз. Помимо количественных изменений, при острых лейкозах встречается такой феномен как лейкемический провал, подразумевающий наличие только зрелых форм лейкоцитов и большого количества бластных клеток, отсутствие промежуточных форм.
Нейтропении
Еще одной причиной моноцитоза, часто наблюдаемой у детей, признаны заболевания, сопровождающиеся снижением (главным образом генетически детерминированным) выработки костным мозгом нейтрофильных гранулоцитов – нейтрофилов. К ним относят циклическую нейтропению, синдром Костмана (детский агранулоцитоз), хроническую нейтропению с нарушением выхода гранулоцитов из костного мозга (миелокахексию). Точный механизм моноцитоза при этих патологиях неизвестен. Обычно наблюдается умеренный моноцитоз в сочетании с эозинофилией.
Редкие причины
- Паразитарные инфекции: висцеральный, кожный лейшманиоз, малярия.
- Отравления: фосфором, тетрахлорэтаном.
- Прием ЛС: длительное введение глюкокортикостероидов.
- Восстановление костномозгового кроветворения: после миелосупрессии химиотерапевтическими препаратами.
Диагностика
Уровень моноцитов измеряется во время подсчета лейкоцитарной формулы в клиническом анализе крови. Обнаружение моноцитоза требует консультации медицинского специалиста, желательно терапевта. Врач должен провести опрос жалоб больного, собрать анамнестические данные, выполнить общий осмотр на предмет выявления признаков того или иного заболевания. Полученные данные служат подспорьем для назначения дополнительного обследования для выяснения причины моноцитоза:
- Анализы крови. В общем анализе крови проводится подсчет общего количества, процентного соотношения всех форм лейкоцитов (лейкоцитарная формула), определяется СОЭ. В мазке крови проверяется наличие атипичных мононуклеаров. Исследуется уровень аутоантител (к ДНК, мышечным клеткам, к топоизомеразе), антигранулоцитарных антител, СРБ. Проводится иммуногистохимический анализ и иммунофенотипирование клеток для выявления поверхностных специфических или опухолевых CD-маркеров.
- Микробиологические исследования. Для идентификации инфекционного возбудителя выполняется бактериологический посев и микроскопия мокроты. Методом иммуноферментного анализа и полимеразной цепной реакции определяются антитела к вирусам, бактериям, их ДНК. Проводятся серологические анализы (реакции непрямой гемагглютинации, микропреципитации).
- Рентгенография. При туберкулезе, саркоидозе на рентгенографии легких обнаруживается увеличение медиастинальных, прикорневых лимфатических узлов, при гистиоцитозе – двусторонние мелкоочаговые затемнения. Также для гистиоцитоза характерны участки остеолизиса и деструкции на рентгенограммах плоских костей черепа, длинных трубчатых костей.
- Сонография. Во время проведения УЗИ брюшной полости у пациентов с инфекционным мононуклеозом, бруцеллезом, онкогематологическими заболеваниями отмечается спленомегалия, реже гепатомегалия. На эхокардиографии у больных коллагенозами иногда удается выявить утолщение листков перикарда, выпот в перикардиальную сумку.
- Гистологические исследования. При злокачественных болезнях крови в мазке костного мозга, полученном путем стернальной пункции либо трепанобиопсии, обнаруживается большое количество бластных клеток. При микроскопическом исследовании бронхоальвеолярной жидкости у пациентов с гистиоцитозом отмечаются гигантские клетки Лангерганса, имеющие эозинофильную цитоплазму. В биоптате лимфоузла при лимфомах выявляются пролиферация лимфоидных клеток, клетки Березовского-Штернберга.
Коррекция
Консервативная терапия
Привести уровень моноцитов к нормальным значениям напрямую невозможно. Для этого необходимо бороться с причиной, т.е. лечить основную патологию, на фоне которой развился моноцитоз. Если моноцитоз обнаружен в крови у человека, недавно перенесшего острое инфекционное заболевание, то лечение не требуется. Это абсолютно нормальное явление, концентрация моноцитов самостоятельно нормализуется через несколько дней. В случае продолжительного и, тем более, высокого моноцитоза, необходимо медицинское вмешательство:
- Противоинфекционное лечение. Для лечения большинства вирусных инфекций достаточно лишь постельного режима, обильного горячего питья, использования нестероидных противовоспалительных препаратов (парацетамол, ибупрофен), а также симптоматической терапии (полоскание или орошение горла антисептическими, обезболивающими растворами, спреями, закапывание в нос сосудосуживающих капель). При бактериальных инфекциях назначаются антибиотики, при туберкулезе – комбинация противотуберкулезных средств.
- Противовоспалительное лечение. В качестве патогенетического лечения хронических гранулематозных заболеваний, коллагенозов используются лекарственные препараты, подавляющие воспаление – глюкокортикостероиды (преднизолон, метилпреднизолон). Для более мощного противовоспалительного действия эффективны иммуносупрессанты – метотрексат, циклофосфамид.
- Химиотерапия. Для лечения злокачественных болезней крови, гистиоцитоза необходимо проведение курсов химиотерапевтического лечения. Иногда приходится прибегать к интратекальному введению препаратов (введению в цереброспинальную жидкость).
Хирургическое лечение
Существует хирургический способ лечения онкогематологических заболеваний и некоторых видов врожденных нейтропений, позволяющий добиться полного исцеления от болезни, – это пересадка донорских гемопоэтических стволовых клеток. Для проведения этой операции необходимо выполнить HLA-типирования (генетический тест, определяющий антигены гистосовместимости) с целью подбора подходящего донора. Однако к данному методу лечения прибегают в крайнем случае при безуспешности консервативной терапии, так как он ассоциирован с высоким риском летального исхода.
Прогноз
Сам моноцитоз не является индикатором прогноза. Исход напрямую определяется причиной моноцитоза. Например, физиологический моноцитоз у детей никак не влияет на продолжительность жизни. Некоторые хронические гранулематозные заболевания, в частности, саркоидоз, иногда даже без всякого лечения заканчиваются самостоятельной ремиссией. Онкогематологические патологии и наследственные нейтропении у детей, напротив, характеризуются неблагоприятным прогнозом и большой вероятностью смерти.
Лимфоцитоз
Лимфоцитоз – это физиологическое состояние организма, когда увеличивается количество лимфоцитов в крови, которая циркулирует по сосудам (периферический кровоток). Лимфоцит – это клетка, которая является разновидностью лейкоцитов агранулоцитного типа – белых кровяных телец. Функции лимфоцитов:
- Иммунный, защитный характер – выработка антител к чужеродным белкам – иммунитет гуморального типа;
- Регуляторный характер – разрушение атипичных клеток, таких как клетки с выраженной онкологией, клетки с мутациями;
- Клеточный иммунитет – контактное взаимодействие с клетками-жертвами – бактериями, вирусами, грибками.
- Норма содержания лимфоцитов относительно общего количества лейкоцитов в крови выглядит так:
- Взрослый человек – 21-38%;
- У детей – от 15% – 35 % (новорождённые) до 30% – 50% (с 6 до 15 лет).
У женщин отмечается отклонение от нормы до 49%-55% в период критических дней или наступления беременности.
Лимфоцитоз у взрослых наблюдается, когда повышается процентное содержание лимфоцитов на 15%. Повышение возникает как ответная реакция на аллерген, стресс или инфекцию. Также своё влияние имеет тип питания и качество окружающей среды.

У детей, возраст которых не превышает 1 год, активно формируется собственная иммунная система. Поэтому содержание лимфоцитов в крови ребёнка доходит до 70%.
Функционально лимфоциты делятся на три группы:
| Т-лимфоциты | В-лимфоциты | NK-лимфоциты | |
| Локализация | Тимус – вилочковая железа. | Костный мозг. В период эмбрионального развития ещё и в печени. | Костный мозг. В малом количестве в селезёнке и лимфатических узлах. |
| Функция | Обеспечивают иммунный ответ через активацию В-лимфоцитов и NK-лимфоцитов. | Обеспечивают гуморальный иммунитет. Распознают чужеродные белки и вырабатывают против них антитела. | Натуральные киллеры. Токсичны для онкологических клеток, собственных клеток организма, которые перенесли мутацию. |
Виды лимфоцитоза
Лимфоцитоз имеет код по МКБ-10 (международная классификация болезней 10-го пересмотра) – D72.8.
Относительный лимфоцитоз
Относительный лимфоцитоз – это явление, при котором лейкоциты находится в пределах нормы в единице объёма крови. При этом количество лимфоцитов в пропорциональном отношении к клеткам того же класса повышено. Такая картина может встречаться как вариант нормы, если анализ сдавал ребёнок в возрасте до двух лет. У детей в процессе развития иммунной системы происходит изменение числа лимфоцитов и нейтрофилов. Это явление носит физиологический характер и называется нейтрофильно-лимфоцитарный перекрёст.
У взрослых такой показатель часто говорит об истощении иммунной системы и является признаком затяжной гнойно-воспалительной болезни – фурункулёза или затяжной пневмонии. При этом количество нейтрофилов падает относительно лимфоцитов, потому что большая часть нейтрофилов уходит в гной и не успевает восстанавливаться. Нейтропения – резкое падение количества нейтрофилов крови.
Если количество лимфоцитов понижено до критического уровня, это лейкопения. Может проявиться при генетическом дефекте, нарушении обмена веществ с недостатком фолиевой кислоты, витаминов группы В и меди, поражениями костного мозга, работой с химическими реактивами – пестицидами, бензолами и т.д.
Если количество лимфоцитов повышено, такая клиническая картина может говорить о:
- спленомегалии – увеличении селезёнки;
- гипертиреозе – выделение гормонов щитовидной железы больше, чем того требует организм;
- болезни Аддисона – надпочечники не вырабатывают необходимое количество гормонов, особенно кортизола.
Гранулопения – пониженное содержание гранулоцитов в кровяном русле. Гранулоцит – это белое кровяное тельце с большим сегментированным ядром. Обеспечивает клеточный иммунитет. Производство угнетается при брюшном тифе и туляремии.
Относительный лимфоцитоз встречается чаще, чем абсолютный.
Абсолютный лимфоцитоз
Абсолютный лимфоцитоз – абсолютное повышение количества лимфоцитов в крови. По типу действия – реактивный лимфоцитоз. Возникает как реакция на другое острое заболевание:
- острые инфекции – ветряная оспа, корь, гепатиты различного генеза, коклюш;
- туберкулёз;
- онкологические болезни – лимфосаркома, лимфолейкоз;
- аутоиммунное заболевание – СПИД.
После устранения причины болезни проходит через 1-2 месяца.
Инфекционный лимфоцитоз
Инфекционный лимфоцитоз появляется при формировании острого поражения организма
Т-лимфотропным вирусом. Т-лимфотропные вирусы – это вирусы из рода дельтаретровирусов, которые вызывают у человека злокачественные образования кроветворной – Т- клеточный лейкоз и лимфоидной тканей – Т- клеточную лимфому. Поражает взрослых людей. Встречается редко.
Онкологический (злокачественный) лимфоцитоз
Злокачественный лимфоцитоз проявляет себя как самостоятельное заболевание лимфопролиферативного профиля – хронический или острый лейкоз.
Причины появления лимфоцитоза
Лимфоциты преимущественно локализуются в костном мозге. Но кроме костного мозга депо лимфоцитов находится также в селезёнке, тонком кишечнике, миндалинах горла, в группах лимфоузлов. При попадании чужеродного патогена в организм следует иммунный ответ – количество белых клеток крови увеличивается.
Инфекции вирусного и бактериологического происхождения – самые распространённые причины лимфоцитоза. К ним также относятся:
- Вирусные инфекции – инфекционный мононуклеоз (болезнь Филатова), гепатит А, острый вирусный гепатит, корь, ОРВИ, ВИЧ, цитомегаловирусная инфекция.
- Бактериальные инфекции – туберкулёз, стафилококки, сифилис, сальмонелла, брюшной тиф, коклюш. Также бруцеллёз – мальтийская лихорадка.
- Болезни, вызванные паразитами – токсоплазмоз.
- Болезни эндокринной системы – гипертиреоз, болезнь Аддисона.
- Ревматические заболевания – подагра, ревматический артрит.
- Болезни лимфатической системы – лимфома, макроглобулинемия Вальденстрема, хронический лимфолейкоз.
- Болезни онкологического происхождения злокачественного и доброкачественного характера, в том числе поражение кроветворных органов.
Среди причин увеличения лимфоцитов в крови не только заболевания. Лимфоцитоз вызывает также:
- Длительное курение табака. У курильщиков уровень лимфоцитов повышен.
- Стресс, провоцирующий гормональные всплески. Сюда относятся критические дни у женщин, тяжёлые физические нагрузки. Если при стрессовой ситуации возникает подсознательная реакция «бей либо беги», то в крови повышается уровень клеток «естественных киллеров». Если такой стресс длится долго и переходит в хроническую форму, появляется обратный эффект – лейкопения. Лимфоцитоз временный, проходит сам.
- Отравление организма тяжёлыми металлами или химическими веществами – свинцом, дисульфидом углерода, мышьяком.
- Удаление селезёнки.
- Лечение некоторыми препаратами – левомицетином, фенитоином, леводопом, глюкокортикоидные лекарства. Или передозировка анальгетиками.
- Истощение организма может характеризоваться упадком сил, вялостью, пониженной температурой.

Симптомы лимфоцитоза
Самостоятельной болезнью не является, кроме инфекционной формы. В большинстве случаев это дополнительный симптом к заболеванию. Поэтому признаками лимфоцитоза выступают симптомы основной болезни, которая вызвала сдвиг в лейкоцитарной формуле.
Назначить лечение может только квалифицированный специалист после полного обследования и установления диагноза.
К симптомам вероятного лимфоцитоза относят:
- Увеличение печени – гепатомегалия, селезёнки – спленомегалия.
- Увеличенные лимфатические узлы – лимфаденопатия.
- Усиленная работа потовых желёз.
- Слабость и утомляемость.
- Резкое изменение температуры тела, которое сопровождается истощением и ознобом.
- Нарушения в работе пищеварительной системы – рвота, тошнота, диарея, запор чередование стула.
- Гипертермия слизистой зева, кашель, насморк, другие симптомы заболевания дыхательных путей.
- Нервное расстройство, отсутствие аппетита, нарушения сна.
- Почти белый кожный покров.
- Увеличение миндалин горла на фоне высокой температуры тела до 40 градусов.
- Увеличен уровень лимфоцитов в костном мозге.
У детей к общим симптомам добавляются вздутие живота, нестабильный стул, приступообразная рвота, высыпания на коже (редко), вялость и плаксивость.
Диагностика
При обращении к терапевту диагностика начинается с физического осмотра и сбора анамнеза. Определить наличие лимфоцитоза можно только с помощью исследований в клинических условиях. Для этого пациент сдаёт кровь на общий клинический анализ крови. Забор материала производить в утренние часы. Перед анализом пациент должен проинформировать лечащего врача о том, какие препараты он принимал в течение суток. Эта информация имеет значение, так как приём некоторых препаратов влияет на уровень лейкоцитов и может исказить результат.

Кроме общего развёрнутого клинического анализа, проводят исследования:
- на наличие антител;
- иммунофенотипирование лимфоцитов для определения структуры клеток и профиля лимфобластов;
- цитологическое исследование тканей лимфоузлов – чтобы исключить злокачественные опухоли;
- миелограмма костного мозга для сравнения с клинической картиной, которую даёт анализ периферической крови;
- если моноциты и лимфоциты превышают нормальные значения, то это даёт повод предположить у пациента миелодиспластический синдром или моноцитарный лейкоз.
Постановка диагноза происходит на основании следующих позиций:
- Рост кровяной лимфоцитарной формулы и уменьшение количества тромбоцитов – тромбоцитопении, говорит о гиперспленизме и аутоиммунной тромбоцитопенической пурпуре. Гиперспленизм – это когда селезёнка быстро утилизирует омертвевшие или отслужившие клетки крови вместе со здоровыми клетками. Тоже является сопровождающим симптомом болезней печени, крови, травм селезёнки и некоторых видов лимфом и лейкозов.
- Лейкопения, которая является симптомом осложнения вирусного заболевания, в том числе туберкулёза.
- Одновременное повышение уровня эритроцитов и лимфоцитов. Наблюдается при бактериальных и вирусных инфекциях, которые сопровождаются обезвоживанием организма – жидкий стул, рвота, повышенная температура тела, лихорадка.
- Дисбаланс при одновременном понижении лимфоцитов и лейкоцитов.
Поскольку лимфоцитоз часто сопровождает заболевания онкологического характера, если отсутствуют клинические симптомы инфекционных болезней, врач назначает дополнительное обследование:
- анализ крови на онкомаркеры;
- томография – компьютерная или магниторезонансная;
- ультразвуковое исследование органов брюшной полости и малого таза;
- рентгенологическое обследование;
- фиброгастродуоденоскопия;
- при обнаруженных образованиях показана биопсия тканей.
Лечение
Лечить следует не сам лимфоцитоз, а заболевание, которое его вызвало. Поскольку, как выше сказано, патология не является самостоятельной болезнью.
Терапии не требует детский физиологический лимфоцитоз. В других случаях лечение назначит врач после диагностики.
При инфекционных болезнях, в зависимости от показаний, назначают антибиотики, противовирусные и противовоспалительные лекарства, сульфаниламиды, при вирусных инфекциях – препараты на основе блокаторов канала-М2 и интерфероне. Возможно назначение противогрибковых лекарств. Показано обильное питье и приём препаратов, которые снимают интоксикацию, устраняют болевой синдром и снижают температуру тела.
При туберкулёзе – специальная специфическая терапия ДОТС + терапия.
При злокачественной опухоли – фунгициды, иммунодепрессанты, антибиотики и цитостатические препараты, химиотерапия, в некоторых случаях пересадка костного мозга.
Профилактика
В качестве профилактики возникновения лимфоцитоза необходимо систематически проводить мероприятия по укреплению иммунитета:
- нормализация режима работы и отдыха;
- отказ от чрезмерного употребления табака и алкоголя;
- соблюдение правил личной гигиены;
- систематические физические нагрузки;
- правильное питание, богатое селеном, цинком, калием, магнием, витаминами;
- ежегодные профилактические осмотры;
- в период сезонных заболеваний нужно избегать мест массового скопления народа, мыть руки после каждого посещения таких мест, пройти курс витаминных препаратов.
Если при медосмотре анализ крови показал сдвиг лейкоцитарной формулы, обнаружился один или комплекс симптомов со слабостью, которую человек не может объяснить, постоянной температурой, следует обратиться к врачу. Вовремя обнаруженное заболевание увеличивает шансы на быстрое выздоровление.
Кроме того, врач может исключить заболевания в принципе и назначить профилактические процедуры, и уровень лимфоцитов сам придёт в норму.
Агранулоцитоз
Что такое агранулоцитоз — причины, симптомы и лечение
Что это такое? Агранулоцитоз – это патологическое состояние, главным диагностическим критерием которого является снижение в общем анализе крови (в формуле) общего уровня лейкоцитов до 1·109/л именно за счет фракции гранулоцитов.
Гранулоциты представляют собой популяцию лейкоцитов, содержащих ядро. В свою очередь, они делятся на три субпопуляции – базофилы, нейтрофилы и эозинофилы. Название каждой из них обусловлено особенностями окрашивания, которые указывают на биохимический состав.
Условно считается, что нейтрофилы обеспечивают антибактериальный иммунитет, эозинофилы – противопаразитарный. Таким образом, главным признаком и наиболее значимым для угрозы жизни больного фактором оказывается резкая утрата способности сопротивляться различным инфекциям.

Причины агранулоцитоза
При аутоиммунной форме синдрома в функционировании иммунной системы происходит определенный сбой, в результате чего она вырабатывает антитела (так называемые аутоантитела), атакующие гранулоциты, вызывая тем самым их гибель.
Общие причины заболевания:
- Вирусные инфекции (вызванные вирусом Эпштейна – Барр, цитомегаловирус, желтая лихорадка, вирусные гепатиты) обычно сопровождаются умеренной нейтропенией, однако в некоторых случаях может развиться агранулоцитоз.
- Ионизирующая радиация и лучевая терапия, химические вещества (бензол), инсектициды.
- Аутоиммунные заболевания (например, красная волчанка, аутоиммунный тиреоидит).
- Тяжелые генерализованные инфекции (как бактериальные, так и вирусные).
- Исхудание.
- Генетические нарушения.
Лекарственные средства могут вызвать агранулоцитоз в результате прямого угнетения кроветворения (цитостатики, вальпроевая кислота, карбамазепин, бета-лактамные антибиотики), либо действуя как гаптены (препараты золота, антитиреоидные препараты и пр.).
Формы
Агранулоцитоз бывает врожденным и приобретенным. Врожденный связан с генетическими факторами и встречается крайне редко.
Приобретенные формы агранулоцитоза выявляются с частотой 1 случай на 1300 человек. Выше описывалось, что, в зависимости от особенностей патологического механизма, лежащего в основе гибели гранулоцитов, выделяют следующие его виды:
- миелотоксический (цитотоксическая болезнь);
- аутоиммунный;
- гаптеновый (лекарственный).
Известна также генуинная (идиопатическая) форма, при которой причину развития агранулоцитоза установить не удается.
По характеру течения агранулоцитоз бывает острым и хроническим.

Симптомы агранулоцитоза
Симптоматика начинает возникать после того, как содержание антилейкоцитарных антител в крови достигнет определенного предела. В связи с этим при появлении агранулоцитоза в первую очередь человека беспокоят такие симптомы:
- плохое общее самочувствие — сильная слабость, бледность и потливость;
- повышенная температура (39º-40º), озноб;
- появление язвочек в полости рта, на миндалинах и мягком нёбе. В этом случае человек чувствует боль в горле, ему трудно глотать, появляется слюнотечение;
- пневмония;
- сепсис;
- язвенные поражения тонкого кишечника. Больной чувствует вздутие живота, у него появляется жидкий стул, схваткообразные боли в животе.
Кроме общих проявлений агранулоцитоза происходят изменения в анализе крови:
- у человека резко снижается общее количество лейкоцитов;
- происходит падение уровня нейтрофилов, вплоть до полного отсутствия;
- относительный лимфоцитоз;
- увеличение СОЭ.
Для подтверждения наличия агранулоцитоза у человека назначают исследование костного мозга. После постановки диагноза начинается следующий этап — лечение агранулоцитоза.
Диагностика агранулоцитоза
Группу потенциального риска по развитию агранулоцитоза составляют пациенты, перенесшие тяжелое инфекционное заболевание, получающие лучевую, цитотоксическую или иную лекарственную терапию, страдающие коллагенозами. Из клинических данных диагностическое значение представляет сочетание гипертермии, язвенно-некротических поражений видимых слизистых и геморрагических проявлений.
Наиболее важным для подтверждения агранулоцитоза является исследование общего анализа крови и пункция костного мозга. Картина периферической крови характеризуется лейкопенией (1-2х109/л), гранулоцитопенией (менее 0,75х109/л) или агранулоцитозом, умеренной анемией, при тяжелых степенях – тромбоцитопенией. При исследовании миелограммы выявляется уменьшение количества миелокариоцитов, снижение числа и нарушение созревания клеток нейтрофильного ростка, наличие большого количества плазматических клеток и мегакариоцитов. Для подтверждения аутоиммунного характера агранулоцитоза производится определение антинейтрофильных антител.
Всем пациентам с агранулоцитозом показано проведение рентгенографии легких, повторные исследования крови на стерильность, исследование биохимического анализа крови, консультация стоматолога и отоларинголога. Дифференцировать агранулоцитоз необходимо от острого лейкоза, гипопластической анемии. Также необходимо исключение ВИЧ-статуса.
Осложнения
Миелотоксическая болезнь может иметь следующие осложнения:
- Пневмония.
- Сепсис (заражение крови). Часто наблюдается сепсис стафилококкового типа. Наиболее опасное осложнение для жизни пациента;
- Прободение в кишечнике. Подвздошная кишка является наиболее чувствительной к образованию сквозных отверстий;
- Тяжёлые отекания слизистой кишки. При этом у пациента наблюдается непроходимость кишечника;
- Острый гепатит. Нередко при лечении образуется эпителиальный гепатит;
- Образование некрозов. Относится к инфекционным осложнениям;
- Септицемия. Чем больше больной болеет миелотоксическим видом болезни, тем тяжелее устранять её симптомы.
Если недуг вызван гаптенами или возникает из-за слабости иммунитета, то симптоматика болезни проявляется наиболее ярко. Среди источников, вызывающих инфекцию, выделяют сапрофитную флору, к которой относят синегнойную или кишечную палочку. При этом у больного наблюдается сильная интоксикация, повышение температуры до 40–41 градусов.

Как лечить Агранулоцитоз?
В каждом конкретном случае учитывается происхождение агранулоцитоза, степень его выраженности, наличие осложнений, общее состояние пациента (пол, возраст, сопутствующие заболевания и т.д.). [adsen]
При обнаружении агранулоцитоза показано комплексное лечение, включающее целый ряд мероприятий:
- Госпитализация в гематологическое отделение стационара.
- Помещение больных в боксированную палату, где регулярно проводится обеззараживание воздуха. Полностью стерильные условия помогут предупредить заражение бактериальной или вирусной инфекцией.
- Парентеральное питание показано больным с язвенно-некротической энтеропатией.
- Тщательный уход за полостью рта заключается в частых полосканиях с антисептиками.
- Этиотропная терапия направлена на устранение причинного фактора — прекращение лучевой терапии и введения цитостатиков.
- Антибиотикотерапия назначается больным с гнойной инфекцией и тяжелыми осложнениями. Для этого используют сразу два препарата широкого спектра — «Неомицин», «Полимиксин», «Олететрин». Лечение дополняют противогрибковыми средствами — «Нистатином», «Флюконазолом», «Кетоконазолом».
- Переливание лейкоцитарного концентрата, пересадка костного мозга.
- Применение глюкортикоидов в высоких дозах — «Преднизолона», «Дексаметазона», «Дипроспана».
- Стимуляция лейкопоэза — «Лейкоген», «Пентоксил», «Лейкомакс».
- Дезинтоксикация — парентеральное введение «Гемодеза», раствора глюкозы, изотонического раствора натрия хлорида, раствора «Рингера».
- Коррекция анемии — напр. для ЖДА препараты железа: «Сорбифер дурулес», «Феррум лек».
- Лечение геморрагического синдрома — переливания тромбоцитарной массы, введение «Дицинона», «Аминокапроновой кислоты», «Викасола».
- Обработка полости рта раствором «Леворина», смазывание язвочек облепиховым маслом.
Прогноз лечения болезни, как правило, благоприятный. Его может ухудшить появление очагов некроза тканей и инфекционных язв.
Меры профилактики
Профилактика агранулоцитоза, главным образом, заключается в проведении тщательного гематологического контроля во время курса лечения миелотоксическими препаратами, исключении повторного приема лекарств, ранее вызвавших у больного явления иммунного агранулоцитоза.
Неблагоприятный прогноз наблюдается при развитии тяжелых септических осложнений, повторном развитии гаптеновых агранулоцитозов
Агранулоцитоз
Агранулоцитоз (алейкия) – это гематологический синдром, характеризующийся полным или почти полным исчезновением гранулоцитов из крови. Впервые описан в 1922 году Шульцем и независимо от него Фридеманом под названием агранулоцитарная ангина.
Причины возникновения
Агранулоцитоз в основном развивается на фоне применения различных видов лекарств, которые могут повредить костный мозг, а именно:
• нестероидные противовоспалительные препараты;
• противопаразитарные препараты, в основном, мебендазол;
• лекарства, используемые для лечения гипертиреоза.
Кроме того, агранулоцитоз может быть вызван химиотерапией и лучевой терапией, апластической анемией, аутоиммунными заболеваниями, а также врожденными факторами, такими как синдром Костмана или циклическая нейтропения. Агранулоцитоз также может быть вызван вирусными инфекциями, миелодиспластическими синдромами, миелофиброзом и лейкемией.
Уменьшение количества лейкоцитов также происходит в процессе трансплантации стволовых клеток, когда костный мозг донора еще не начал работать и костный мозг реципиента уже полностью разрушен. Тем не менее, это ожидаемый и переходный процесс, который длится несколько дней. В течение этого времени пациенту помогают гранулоцитарные колониестимулирующие факторы.
Другой причиной агранулоцитоза может быть повреждение костного мозга вследствие отравления токсичными веществами, такими как бензол, тринитротолуол, гербициды и инсектициды, а также тяжелые металлы. Исследования также показывают, что употребление кокаина может привести к агранулоцитозу.
Механизм развития болезни
Многие, главным образом лекарственные формы гранулоцитопений и агранулоцитозов, рассматриваются как иммуно-аллергические, возникающие под влиянием антилейкоцитарных антител.
Согласно теории иммуногенеза лейкопенических состояний и агранулоцитозов, первичные изменения касаются периферической крови, изменения же костного мозга являются вторичными, которые возникают в ответ на массовый лейколиз. Общепризнанная в настоящее время возможность иммуногенных агранулоцитозов, особенно медикаментозной этиологии, протекающих по пластическому варианту, доказывается обнаружением в крови специфических антилейкоцитарных антител, а также положительными результатами лечения стероидными гормонами. Это не исключает существования агранулоцитозов, возникающих в результате непосредственного влияния патогенного агента на костномозговое кровотворение. К таковым относятся главным образом агранулоцитозы бензольной, злаковой, хлорэтиламиновой и лучевой этиологии, протекающие с картиной «опустошенного» костного мозга.
Таким образом, исходя из современных представлении о патогенезе агранулоцитозов, следует выделить две основные группы гранулоцитопений:
При этом развязывание агранулоцитарного синдрома по типу «гемоклазического криза» с явлениями анафилактоидного порядка (повышение температуры с ознобом, боли в суставах, местный аллергический отек) может наблюдаться и без участия медикаментозного фактора.
Пусковой механизм, приводящий к образованию антилейкоцитарных антител, в большинстве случаев остается неизвестным. Ясно только то, что аутоагрессивный конфликт возникает в результате накопления в организме антилейкоцитарных антител, приводящих к массовому лизису лейкоцитов.
В зависимости от симптоматики и преимущественной локализация процесса можно выделить следующие клинические формы агранулоцитоза:
Следует добавить, что последние две формы – кишечная и легочная, чаще всего сочетаются с первой. Вообще агранулоцитарный синдром редко развивается без поражения полости рта и глотки.
Симптомы и клиническая картина
Клиническая картина чаще всего выражается в язвенно-некротических поражениях полости рта и миндалин. Возникновению типичных симптомов агранулоцитоза предшествует латентный период, который характеризуется недомоганием, потерей аппетита, головной болью. Исследование крови в этот период обнаруживает прогрессирующую лейкопению. При агранулоцитозах лекарственно-токсической этиологии продромальный период весьма непродолжителен: типичная картина может развиться уже на следующий день после приема препарата.
В разгар агранулоцитоза наблюдается резкая слабость и лихорадка, большей частью ремиттирующего характера; одновременно развиваются некротические явления в глотке: появляется боль в горле, затрудняется речь и глотание.
У больных отмечается резкая бледность, изредка – иктеричность, иногда – герпес. На миндалинах обнаруживается грязно-серый налет, в некоторых случаях типично дифтеритический; в дальнейшем образуются некротические бляшки и язвы. Распространяясь вширь, некротизация захватывает небные дужки, язычок, десны, мягкое и твердое нёбо; реже в процесс вовлекаются слизистые губ, языка и полости рта; распространяясь вглубь, процесс принимает характер номы. При разрушении глубжележащих сосудов возникает обильное кровотечение.
Иногда наблюдается незначительное увеличение регионарных лимфоузлов, главным образом шейных и подчелюстных. Агранулоцитарная ангина является классической формой агранулоцитоза, однако язвенно-некротический процесс при агранулоцитозе может поражать и другие органы (известны случаи легочной гангрены). Другим избирательным местом некротического процесса является кишечник. Кишечная форма агранулоцитоза дает тифоподобную картину болезни. Некротический процесс, локализующийся, как при брюшном тифе, в области пейеровых бляшек толстых кишок, достигает особой интенсивности, приводя к кровотечениям и перфорации кишечника. Некрозы могут локализоваться и в пищеводе, толстом кишечнике, на месте перехода слизистой прямой кишки в кожу вокруг анального отверстия и на самой коже, а также в мочевом пузыре, женских половых органах и т. д.
В сердечно-сосудистой системе особых изменений нет, за исключением гипотонии (артериальной и венозной) и анемических сердечных и сосудистых шумов. Селезенка, как правило, не увеличена. При развитии геморрагического синдрома появляется гематурия.
Больные апатичны, но сохраняют сознание вплоть до агонии.
• Изменения крови . Уже в первоначальной, лейкопенической стадии болезни наблюдается прогрессирующая нейтропения. В дальнейшем, язвенно-некротическом периоде болезни изменения крови характеризуются более резким падением нейтрофилов вплоть до их полного исчезновения. Степень агранулоцитоза и быстрота его развития соответствуют тяжести процесса. Эозинофилы в некоторых случаях сохраняются и нормальном и даже повышенном количестве.
В уцелевших гранулоцитах обнаруживаются дегенеративные изменения ядра и протоплазмы; в последней появляется токсогенная зернистость. В некоторых случаях на высоте агранулоцитоза наблюдается моноцитарная реакция с появлением большого количества моноцитов гистогенной природы. Нередко в крови встречаются лимфоидные ретикулярные и плазматические клетки.
В тяжелых случаях с летальным исходом изменения крови прогрессируют до самой смерти больного. При затяжном течении костный мозг постепенно выходит из состояния первоначального торможения.
После перелома в течении болезни нередко наблюдается лейкемоидная реакция с появлением молодых форм гранулоцитов – миелоцитов, промиелоцитов и даже единичных миелобластов. Позже, по мере выздоровления, картина крови становится нормальной.
Красная кровь при «чистых» формах агранулоцитоза не представляет особых изменений или дает картину умеренной анемии. В случае присоединения геморрагий анемия усиливается.
Количество тромбоцитов при «чистых» формах агранулоцитоза изменяется мало. В более тяжелых случаях развивается резкая тромбоцитопения с геморрагическим синдромом – так называемая геморрагическая алейкия, или «злокачественная» тромбоцитопения.
• Костный мозг . По состоянию костномозгового кроветворения следует различать пластические и апластические формы агранулоцитоза.
Пластические формы по картине периферической крови соответствуют истинному агранулоцитозу, но отличаются кратковременным и доброкачественным течением. При этом в пункте костного мозга отмечается сдвиг влево в гранулоцитарном ряду при уменьшении числа зрелых форм – палочкоядерных и сегментоядерных нейтрофилов. В происхождении подобных гранулоцитопений основную роль играет нарушенное вызревание мета-миелоцитарных клеток в костном мозгу. Развитие последних обрывается па стадии промиелоцитов (так называемый промиелоцитарный костный мозг).
При апластической форме исчезают и промиелоциты, и в костном мозгу сохраняются лишь в небольшом проценте миелобласты; преобладают же ретикулярные и плазматические клетки (лимфоидно-ретикулярный костный мозг). Все же такой костный мозг способен к полной репарации. В других случаях отмечается полное опустошение активного костного мозга, который замещается жировой тканью (жировой костный мозг). Эритробластический росток костного мозга при пластических формах агранулоцитоза не страдает.
При апластических агранулоцитозах, протекающих с анемией, эритробластический росток костного мозга поражен в той же мере, как и лейкобластический; процесс дифференциации эритробластов резко нарушается. Последними исчезают из костного мозга мегакариоциты. При этом прекращается процесс образования тромбоцитов и развивается тромбоцитопения.
Наряду с исчезновением кроветворном ткани костного мозга в нем наблюдается пролиферация ретикулярных элементов. Среди последних можно выявить три типа клеток:
1) лимфоидные ретикулярные клетки, которые встречаются нередко в виде синцитиальных скоплений без ясных клеточных границ;
2) плазматические ретикулярные клетки в различных стадиях развития;
3) макрофаги, то есть ретикулярные клетки в состоянии активного фагоцитоза.
Клетки эти неправильной формы, широкопротоплазменные, с малым, круглым или овальным, эксцентрически расположенным ядром; в светло-голубой протоплазме содержатся азурофильные зерна, жировые капли, фагоцитированные ядра, эритроциты и глыбки пигмента. По мере накопления (инфильтрации) жировых капель в макрофаге последний превращается и жировую клетку. Иногда в связи с жировым перерождением большинства ретикулярных клеток наблюдается превращение лимфоидно-ретикулярного костного мозга в жировой.
Патологоанатомическая картина
Гистологическая картина органов характеризуется отсутствием демаркационного вала по периферии язвенно-некротических участков. Несмотря на наличие в пораженных органах обильной бактериальной флоры, признаки воспалительной реакции отсутствуют: нет лейкоцитарной реакции и нагноения. На границе с некротическими участками отмечается лишь скудное количество моноцитов, лимфоцитов и плазмоцитов. При развитии анемии и геморрагического синдрома (апластические формы) обнаруживаются геморрагии в органах, их ишемия и жировая инфильтрация.
Состояние костного мозга при пластических и апластических формах агранулоцитоза различно: в первом случае он сохранен, но кроветворение находится в состоянии функционального угнетения, во втором имеется картина ретикулярного костного мозга с переходом в опустошенный костный мозг – панмиелофтиз. При этой форме в кроветворных органах нередко наблюдаются миелоидные очаги, которые можно рассматривать как неполноценную компенсацию кроветворения. Внекостномозговая миелоидная метаплазия наблюдается главным образом в селезенке, лимфоузлах и печени. Однако следует иметь в виду, что в отличие от истинного миелоза миелоидная метаплазия при агранулоцитозе имеет весьма ограниченное распространение.
Дифференциальная диагностика
Наибольшие трудности для отличия от агранулоцитоза представляет лейкопеническая форма острого лейкоза.
Стернальная пункция, устанавливающая тотальную гемоцитобластную метаплазию костного мозга, точно решает диагноз в пользу лейкоза. Такой метаплазии при алейкии никогда не наблюдается. При последней отмечается в основном опустошенный ретикулярный костный мозг, па фоне которого могут попадаться лишь единичные гемоцитобласты.
Возможны и такие случаи, когда в начале заболевания наблюдается агранулоцитоз, а в дальнейшем развивается острейшая лейкемия. Их следует трактовать не как переход одного заболевания в другое, а как смену лейкопенической, агранулоцитарной фазы гемоцитобластного лейкоза лейкемической стадией.
Лечение
Основным принципом лечения агранулоцитозов является комплексность и неотложность лечебных мероприятий, проводимых с учетом этиологии и патогенеза страдания, а также состояния костномозгового кроветворения.
В случае известной этиологии нужно устранить причину, которая вызвала агранулоцитоз: отменить токсические и аллергизирующие препараты, убрать воздействие ионизирующей радиации и т. п. Вместе с тем независимо от этиологии и патогенеза страдания следует считать обязательным для каждого больного агранулоцитарным синдромом следующий комплекс лечебных средств: гемотерапия, гемостимуляторы, гипофизарно-надпочечниковые гормоны и антибиотики.
• Гемотерапия
Следует учесть, что переливание цельной крови в остром периоде болезни нередко сопровождается тяжелыми реакциями. Более показанными являются переливания раздельных фракций крови – лейкоцитной, эритроцитной и, в случае присоединяющихся тромбоцитопенических кровотечений, тромбоцитной массы. Наиболее эффективными в остром периоде болезни следует считать переливания лейкоцитной массы, производимые по 40-80 мл через 1-2 дня. Аналогичным эффектом обладает лейкоцитная взвесь, приготовленная по методике ЛИПК из обогащенной лейкоцитами плазмы и вводимая в том же количестве по мере требования, то есть в день ее изготовления. В 40 мл лейкоцитной массы (взвеси) должно содержаться не менее 1-2 млрд. жизнеспособных лейкоцитов.
Введение лейкоцитной массы (взвеси) производится повторно, до кровяной ремиссии, наступающей обычно через 1,5-2 недели. Следует помнить о возможности возникновения изоиммунных антител в связи с повторными инфузиями донорских лейкоцитов. По этой причине предпочтительно введение лейкоцитов одноименной группы. В период реконвалесценции, при наличии некоторой анемизации, а также в случаях нетяжелой гранулоцитопении рекомендуется произвести 1-2 переливания эритроцитной массы по 150-200 мл.
• Гемостимуляторы
С успехом применяют получаемую из дрожжей 5% натриевую соль нуклеиновой кислоты (рибонуклеиновой кислоты), содержащей пуриновые (аденин, гуанин) и пиримидиновые основания. Нуклеиновокислый натрий вводят детям в 1-2% растворе (0,5-5 мл), а взрослым – в 5% растворе (5-10 мл) внутримышечно 1-2 раза в день в течение 10-15 дней, то есть до наступлении ремиссии. Учитывая «беззащитность» больного в период полного агранулоцитоза, следует во избежание местных осложнений (некрозов) соблюдать строжайшую асептику при внутримышечных введениях препаратов нуклеиновой кислоты.
Эффективность стимуляторов лейкопоэза весьма относительна и зависит в основном от формы процесса, его принципиальной обратимости. Терапевтический аффект в связи с применением указанных препаратов наступает и основном при пластических формах агранулоцитоза. При апластической форме аффект непостоянен. Более эффективными являются витамины группы В, влияющие на интимные процессы нуклеотидного обмена и тем самым стимулирующие клеточную дифференциацию.
• Гипофизарно-надпочечниковые гормоны
Наиболее обоснованным является применение гипофизарно-надпочечниковых гормонов – АКТГ, кортизона, прединзона. Действие гормональных препаратов состоит не только в их подавляющем влиянии на образование аутоагрессивных антител (по этой причине назначение стероидных гормонов при иммуно-аллергических гранулоцитопениях и агранулоцитозах следует рассматривать как патогенетическое), но и в общем тонизирующем эффекте и снижении сосудистой проницаемости (что имеет особое значение в случае присоединяющейся тромбоцитопении и угрожающих геморрагий). В остром периоде показаны большие дозы гормонов: 60-80 единиц АКТГ, 200-250 мг кортизона или 50-100 мг преднизона. С появлением нормального лейкоцитоза, наступающего обычно недели через две от начала лечения, дозировка гормональных препаратов сокращается примерно наполовину. В случаях иммуно-аллергической гранулоцитопении гормональное лечение рекомендуется проводить в течение длительного времени – до наступления полного клинического и «биологического» выздоровления, то есть до исчезновения аутоиммунных антител.
• Антибиотики
Антибиотики назначают в больших дозах с первого момента проявлений агранулоцитоза. Можно рекомендовать примерно следующую схему лечения: инъекция пенициллина по 800000-1200000 единиц, стрептомицина и тетрациклина по 1 г в день. Указанные дозы вводят ежедневно в два приема до наступления клинической и гематологической ремиссии.
Обязательно местное лечение полости рта и глотки путем полосканий растворами грамицидина (одна ампула в 1 мл на полстакана воды), фурациллина (1:5000), риванола, марганцовокислого калия, перекиси водорода.
Прогноз
Прогноз агранулоцитоза определяется многими факторами: степенью интоксикации организма, состоянием нервной и сердечно-сосудистой системы, анатомическим поражением органов, но в основном – степенью поражения костного мозга. При пластических формах агранулоцитоза (особенно при лекарственных – пирамидоновой, атофановой, сульфаниламидной и пр.) прогноз более благоприятный. В редких случаях может наступить смерть от осложнений (сепсис, асфиксия от отека пораженной некротическим процессом гортани).
При апластических формах (с развитием ретикулярного костного мозга) прогноз более серьезен; нелеченые больные нередко умирают от сепсиса, кровотечений. При условии своевременного применения современных средств лечения исход обычно бывает благоприятным.
В случае выздоровления последнее наступает параллельно улучшению картины крови. Некротические участки в горле и в других местах подвергаются обратному развитию и рубцеванию.
Профилактика
Профилактика возможна лишь при агранулоцитозах известной этиологии и заключается в индивидуальном ограждении заболевшего или находящегося в продромальном (лейкопеническом) периоде от соответствующего вредоносного агента.
Лицам, болевшим ангранулоцитозом вследствие приема того или иного препарата, последний вновь назначать нельзя.
Гранулоциты

Гранулоциты (зернистые лейкоциты) – группа белых кровяных клеток, которые в своей цитоплазме содержат гранулы. Пониженное или повышенное количество данного компонента в крови является признаком развития определенного патологического процесса, но установить это можно только путем проведения диагностических мероприятий.
Лейкоциты, то есть белые клетки, в крови разделяются на два типа – гранулоциты и агранулоциты. К первой группе относятся компоненты, которые включают в себя цитоплазму с гранулами. Сегментоядерные гранулоциты очень важны для организма, так как относятся к первой линии защиты от микробов: при образовании очага воспаления именно гранулоциты начинают реакцию иммунного ответа организма.
Причины того, что гранулоциты повышены или понижены, могут быть не только в патологических процессах, но и в факторах внешней среды. Так, спровоцировать отклонение от нормы может прием препаратов или частые стрессы. Контролировать данные показатели в крови у детей или у взрослых очень важно, так нарушение баланса может привести к довольно серьезным осложнениям.
Образование и жизненный цикл
Гранулоциты образуются в костном мозге: клетки делятся в течение четырех дней, после чего происходит их морфологическое дозревание. Данный этап длится не более пяти дней. После того как клетки выходят в кровяное русло, происходит их деление на два вида: пристеночные, которые временно крепятся к стенкам сосудов, и активно циркулирующие. По кровеносной системе они циркулируют около недели, затем выходят в ткань. Здесь клетки живут около двух суток, после чего происходит завершение их жизненного цикла.
Количество гранулоцитов в крови составляет около 60% от общего количества белых клеток. Данные компоненты, в свою очередь, делятся на подвиды.
Таким образом, к гранулоцитам относятся следующие клетки:
- Нейтрофильные гранулоциты – их количество у взрослого или ребенка в крови самое большое. По сути, нейтрофильные гранулоциты обезвреживают патогенные организмы, «жертвуя» собой.
- Базофилы – клетки мгновенно реагируют на аллергены, ускоряют кровообращение и направляют большое количество жидкости на пораженный участок.
- Эозинофильные гранулоциты – воздействуют на паразитарные организмы, предупреждают развитие аллергической реакции. Среди белых телец это самые маленькие и самые подвижные тельца.
Если те или иные гранулоциты понижены или повышены, это может негативно сказаться на работе организма, например, при попадании патогенных организмов иммунная реакция может быть слишком слабой, что приведет к серьезным осложнениям.

Функции
Основные функции гранулоцитов заключаются в формировании иммунной реакции при попадании в организм вируса, паразита, аллергена или любого другого патогенного тела.
Кроме этого, некоторые подвиды белых телец отвечают за ускорение кровообращения при ранении, что помогает предотвратить большую кровопотерю. В целом данный компонент отвечает за полноценное функционирование внутренних органов.
Норма
Норма гранулоцитов будет зависеть от возраста и половой принадлежности человека.
Оптимальными показателями являются следующие:
- у ребенка до месяца гранулоциты норма – 5,5-12,5 10 9 клеток/л
- у ребенка до 12 лет – 4,5-10,0 10 9 клеток/л;
- у ребенка в пубертатный период – 4,3-9,5 10 9 клеток/л;
- в крови у женщин и у мужчин – 1,2-6,8 10 9 клеток/л.
Следует отметить, что повышение гранулоцитов при беременности – это нормальный физиологический процесс и патологией не является. Однако, если показатели существенно выше предельной границы, то обязательно следует пройти полное обследование, на основании которого врач поставит диагноз и назначит корректное лечение.
Возможные причины отклонения от нормы
Причины повышения количества белых телец в крови могут быть следующие:
- паразитарные инфекции;
- острые воспалительные процессы;
- инфекционные заболевания;
- патологические процессы, которые сопровождаются некротизацией тканей;
- аллергические реакции;
- интоксикация организма;
- острые геморрагии;
- болезни кроветворной системы;
- онкологические заболевания;
- воспалительные процессы в желудочно-кишечном тракте;
- синдром Ходжкина;
- нарушения эндокринного характера;
- заболевания сердечно-сосудистой системы;
- гемолитическая анемия;
- инфекционные процессы непаразитарной природы.
Привести к тому, что гранулоциты в крови будут выше нормы, может и прием некоторых медикаментозных препаратов. Как правило, после отмены медикаментов показатели приходят в норму.
Причины того, что гранулоциты в крови ниже нормы, следующие:
- аллергические реакции;
- гастроэнтерологические заболевания;
- системные или аутоиммунные заболевания;
- различные виды анемии;
- скарлатина;
- ревматизм;
- саркоидоз.
Следует учитывать и то, что при расшифровке анализа принимаются во внимание и другие показатели крови, поэтому самостоятельно трактовать данные не рекомендуется: правильно это может сделать только врач.
Проведение анализа
Для того чтобы определить количество белых телец в крови, проводится общий клинический анализ биологической жидкости путем пункции из пальца. Следует отметить, что на результаты могут повлиять и внешние факторы: неправильное проведение процедуры забора жидкости, нарушение техники проведения анализа, неподготовленный пациент. Поэтому, если результаты будут показывать существенное отклонение от нормы, врач может назначить повторное проведение лабораторного исследования.
Контролировать показатели гранулоцитов в крови очень важно, так как от них зависит состояние иммунной системы. Поскольку симптоматически заметить отклонение от нормы не всегда представляется возможным, в целях профилактики необходимо периодически проходить медицинский осмотр со сдачей лабораторных анализов. Любое заболевание гораздо легче предотвратить, чем устранять его последствия.